题目内容
【题目】根据下列装置,结合所学化学知识回答下列问题。

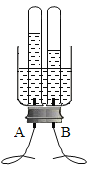
(1)请写出图中标号仪器的名称:① _____________;②____________。
(2)实验室用双氧水与二氧化锰混合制氧气的符号表达式是_____________,发生装置应选用_____(填编号),该装置的优点是__________
(3)实验室用高锰酸钾制取氧气的符号表达式____________,用此方法来制取和收集相对纯净的氧气可用装置____(填编号)。实验过程中发现水槽中的水红了,可能原因是__________。除上述制氧气的方法外,工业上获得氧气的方法是________。
(4)实验室用高锰酸钾制取氧气反应结束后冷却,对制取氧气后的固体残渣(假定已完全反应)作如下回收处理(提示:锰酸钾能溶于水,二氧化锰难溶于水)
①通过以下四步实验操作回收二氧化锰。正确操作的先后顺序是__________(填写序号)。
A 烘干 B 溶解 C 过滤 D 洗涤
②过滤时需用到的玻璃仪器有:_________、烧杯、 玻璃棒,玻璃棒的作用是_________
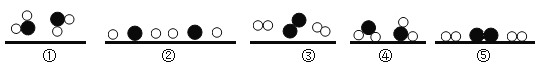
③过滤时需将圆形滤纸折叠。下列滤纸折叠过程图示中,正确的是___________(选填“甲”或“乙” )。

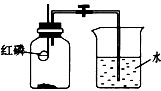
(5)加热碳酸氢铵可得到二氧化碳,能否用加热碳酸氢铵的方法来制备二氧化碳?_____(填“能”或“否”),原因是________。
【答案】长颈漏斗 试管 H2O2![]() H2O+O2 B 能控制反应的速率 KMnO4
H2O+O2 B 能控制反应的速率 KMnO4![]() K2MnO4+MnO2+O2 F 试管口没有放一团棉花 分离液态空气法 BCDA 玻璃棒 引流 甲 否 制备的CO2中混有氨气
K2MnO4+MnO2+O2 F 试管口没有放一团棉花 分离液态空气法 BCDA 玻璃棒 引流 甲 否 制备的CO2中混有氨气
【解析】
(1)长颈漏斗方便加液体药品,试管是常用的反应容器,故答案为:长颈漏斗;试管。
(2)过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的表达式是:H2O2![]() H2O+O2;反应物是双氧水,二氧化锰作催化剂,属于固液常温型,故选发生装置B,该装置的优点是能控制反应的速率;
H2O+O2;反应物是双氧水,二氧化锰作催化剂,属于固液常温型,故选发生装置B,该装置的优点是能控制反应的速率;
故填:H2O2![]() H2O+O2;B;能控制反应的速率。
H2O+O2;B;能控制反应的速率。
(2)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;排水法收集的氧气相对纯净;实验过程中发现水槽中的水红了,可能原因是试管口没有放一团棉花;除上述制氧气的方法外,工业上获得氧气的方法是分离液态空气法。
故填:KMnO4![]() K2MnO4+MnO2+O2;F;试管口没有放一团棉花;分离液态空气法。
K2MnO4+MnO2+O2;F;试管口没有放一团棉花;分离液态空气法。
(4)锰酸钾易溶于水,二氧化锰不溶于水,因此回收二氧化锰的方法是:溶解、过滤、洗涤、干燥;过滤时需用到的实验仪器有:铁架台(带铁圈)、漏斗(带滤纸)、烧杯、玻璃棒;玻璃棒的作用是引流;滤纸折叠的方法中,甲正确;
故填: BCDA;玻璃棒;引流;甲。
(5)不能用加热碳酸氢铵的方法来制备二氧化碳,因为制备的CO2中混有氨气;故答案为:否;制备的CO2中混有氨气。