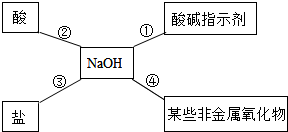
题目内容
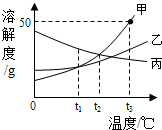 如图是甲、乙、丙三种固体物质的溶解度曲线,请根据图示填空:
如图是甲、乙、丙三种固体物质的溶解度曲线,请根据图示填空:(1)在
(2)在t3℃时,把30g甲溶解于50g水中得到
(3)t1℃时,甲、乙、丙三种物质的饱和溶液中,溶质质量分数的大小关系是
考点:固体溶解度曲线及其作用,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)溶解度曲线的交点表示该温度下两物质的溶解度相等;
(2)据该温度下甲的溶解度分析解答;
(3)据饱和溶液中溶质的质量分数的计算式
×100%分析解答.
(2)据该温度下甲的溶解度分析解答;
(3)据饱和溶液中溶质的质量分数的计算式
| 溶解度 |
| 溶解度+100g |
解答:解:(1)在t2℃时,甲与丙的溶解度曲线交于一点,表示该温度下二者的溶解度相等;
(2)在t3℃时甲的溶解度是50g,即100g水中最多溶解50g的甲,所以把30g甲溶解于50g水中最多溶解25g,得到75g溶液;
(3)据饱和溶液中溶质的质量分数的计算式
×100%可知:溶解度大则溶质的质量分数大,t1℃时,甲、乙、丙三种物质的溶解度大小关系是:丙>甲=乙,所以该温度下的饱和溶液中,溶质质量分数的大小关系是丙>甲=乙;
故答案为:(1)t2;(2)75;(3)丙>甲=乙.
(2)在t3℃时甲的溶解度是50g,即100g水中最多溶解50g的甲,所以把30g甲溶解于50g水中最多溶解25g,得到75g溶液;
(3)据饱和溶液中溶质的质量分数的计算式
| 溶解度 |
| 溶解度+100g |
故答案为:(1)t2;(2)75;(3)丙>甲=乙.
点评:了解溶解度曲线的意义、溶解度概念的含义和饱和溶液中溶解度大则溶质的 质量分数大这些知识,才能结合题意灵活分析解答.

练习册系列答案
相关题目
爱护水资源人人有责.下列日常生活行为不利于保护水资源的是( )
| A、加大施用农药、化肥力度以提高蔬菜产量,满足日常生活需要 |
| B、少用或不用含磷洗衣粉可有效防止水体富营养化 |
| C、在灌溉农田、草坪时,应大力提倡滴灌或喷灌 |
| D、将工业用水沉降、过滤后再利用,虽然成本高,但也值得提倡 |
在一密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下存在某个反应,测得反应前后各物质的质量如下表:对该反应,下列描述正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前物质/g | 20 | m | 20 | 20 |
| 反应后物质/g | 2 | 待测 | 32 | 26 |
| A、该反应中甲、丙、丁的质量比为1:16:13 |
| B、乙在该反应中一定是催化剂 |
| C、待测质量一定为4g |
| D、该反应是分解反应 |
下列有关的化学用语表达正确的是( )
| A、三个水分子:3H2O |
| B、五个氢原子:H5 |
| C、两个钙离子:2Ca+2 |
| D、四个铵根离子:4NH3+ |
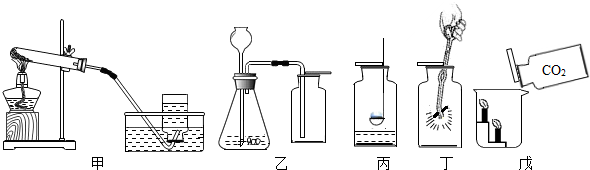
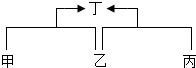 已知甲、乙、丙、丁是初中化学中的四种常见物质,丁是甲与乙、乙与丙反应的生成物之一(反应条件均已略去),转化关系如图:
已知甲、乙、丙、丁是初中化学中的四种常见物质,丁是甲与乙、乙与丙反应的生成物之一(反应条件均已略去),转化关系如图: