题目内容
18.下列物质的用途中,利用其物理性质的是( )| A. | 氧气可用于供给呼吸 | B. | 金属铜用于制导线 | ||
| C. | 碳酸氢钠用于治疗胃酸过多症 | D. | 盐酸用于除铁锈 |
分析 物质在化学变化中表现出来的性质叫化学性质,物质不需要发生化学变化就表现出来的性质,叫物理性质;物理性质经常表现为:颜色、状态、气味、密度、硬度、熔点、沸点、导电性、导热性、溶解性、挥发性等.
解答 解:A、氧气可用于供给呼吸,属于氧气的化学性质,故选项错误;
B、金属铜用于制导线,导电性属于物理性质,故选项正确;
C、碳酸氢钠用于治疗胃酸过多症,属于化学性质,故选项错误;
D、盐酸用于除铁锈,属于盐酸的化学性质,故选项错误;
故选B
点评 本考点考查了物理性质和化学性质的区分,要记忆有关氧气、铜、碳酸氢钠和盐酸的性质,并能够在比较的基础上进行应用,本考点的基础性比较强,主要出现在选择题和填空题中.

练习册系列答案
相关题目
8.下列变化属于化学变化的是( )
| A. | 石蜡熔化 | B. | 粮食酿酒 | C. | 酒精挥发 | D. | 干冰升华 |
6.下列有关检验、鉴别和除杂的实验方案正确的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 检验CO2气体 | 用燃着的小木条放在集气瓶口 |
| B | 除去CuO中混有的少量Cu | 加过量的稀盐酸,充分反应后过滤 |
| C | 除去NaN03溶液中混有的少量NaCl | 加过量AgN03溶液,充分反应后过滤 |
| D | 区分硝酸铵和尿素 | 加熟石灰研磨,闻气味 |
| A. | A | B. | B | C. | C | D. | D |
13.在一次实验课上,各小组同学利用不同地点采集的石灰石与稀盐酸反应制取二氧化碳.小明发现,不同组反应产生气体的速率不一样.于是,各小组同学对影响产生二氧化碳速率的因素进行了如下实验探究:
【设计实验】实验装置如图一所示:
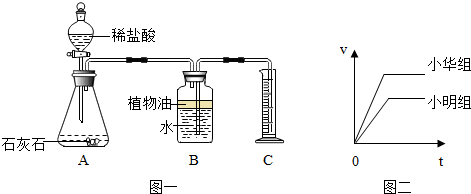
【实验一】探究不同地点采集的石灰石对反应速率的影响分别取出形状相同、质量相同、地点不同的石灰石,加入质量相同、溶质质量分数也相同的稀盐酸进行实验.生成二氧化碳的体积(v)与反应时间(t)的关系如图二所示:
(1)反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)实验结论:①小华组反应产生气体的速率较快.
②小明组产生气体的体积较小(填“大”或“小”),说明小明组采集的石灰石中碳酸钙含量较低(填“高”或“低”).
【实验二】探究不同溶质质量分数的盐酸对反应速率的影响.
小军用不同质量分数的盐酸和各方面都相同的石灰石进行如下实验.
(3)从上述实验中得出不同溶质质量分数的盐酸对反应速率影响的结论是盐酸溶质质量分数越大,反应速率越大.
(4)如果反应时间充足,且所用盐酸是足量的,那么理论上两组实验反应所得到的二氧化碳气体的体积是(填“是”或“否”)相同的.
【问题与讨论】
(5)图一装置气密性检查的方法:用手指把装置C中的导管口堵住,往分液漏斗中加水,打开分液漏斗中加水,打开分液漏斗的活塞,如果分液漏斗内形成稳定的水柱,则图一装置的气密性好.
(6)同学们用图一装置B收集二氧化碳气体,其中油层的作用是防止二氧化碳溶于水,该装置中量筒的作用是通过测量流入水的体积来测量生成二氧化碳气体的体积.
(7)你认为影响产生二氧化碳速率的因素还可能是(写一个):石灰石的形状(或石块质量不同、盐酸质量不同、温度),请写出验证的实验方案:别取质量相同、地点相同、形状大小不同的石灰石,加入质量相同、溶质质量分数相同的盐酸进行实验.测量相同时间内产生而氧虎滩气体的体积.
【设计实验】实验装置如图一所示:

【实验一】探究不同地点采集的石灰石对反应速率的影响分别取出形状相同、质量相同、地点不同的石灰石,加入质量相同、溶质质量分数也相同的稀盐酸进行实验.生成二氧化碳的体积(v)与反应时间(t)的关系如图二所示:
(1)反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)实验结论:①小华组反应产生气体的速率较快.
②小明组产生气体的体积较小(填“大”或“小”),说明小明组采集的石灰石中碳酸钙含量较低(填“高”或“低”).
【实验二】探究不同溶质质量分数的盐酸对反应速率的影响.
小军用不同质量分数的盐酸和各方面都相同的石灰石进行如下实验.
| 实验编号 | 盐酸的质量分数(均取15g) | 相同石灰石(均取1g) | 二氧化碳的体积(mL)(均收集1分钟) |
| 实验Ⅰ | 5% | 石灰石 | 86.3 |
| 实验Ⅱ | 10% | 石灰石 | 152.7 |
(4)如果反应时间充足,且所用盐酸是足量的,那么理论上两组实验反应所得到的二氧化碳气体的体积是(填“是”或“否”)相同的.
【问题与讨论】
(5)图一装置气密性检查的方法:用手指把装置C中的导管口堵住,往分液漏斗中加水,打开分液漏斗中加水,打开分液漏斗的活塞,如果分液漏斗内形成稳定的水柱,则图一装置的气密性好.
(6)同学们用图一装置B收集二氧化碳气体,其中油层的作用是防止二氧化碳溶于水,该装置中量筒的作用是通过测量流入水的体积来测量生成二氧化碳气体的体积.
(7)你认为影响产生二氧化碳速率的因素还可能是(写一个):石灰石的形状(或石块质量不同、盐酸质量不同、温度),请写出验证的实验方案:别取质量相同、地点相同、形状大小不同的石灰石,加入质量相同、溶质质量分数相同的盐酸进行实验.测量相同时间内产生而氧虎滩气体的体积.
10.向黑色固体氧化铜和铁粉的混合物中加入一定量的稀硫酸,充分反应后过滤.以下判断不正确的是( )
| A. | 滤渣中可能含有铜 | B. | 滤渣中可能含有氧化铜 | ||
| C. | 滤液中一定含有硫酸亚铁 | D. | 滤液中不可能含有硫酸铜 |
8.小立在家洗衣服时,发现一瓶刚过期的漂白液,对漂白液的漂白原理和该漂白液是否还有漂白作用产生了疑问.于是将其带到学校,在老师指导下,与小组同学一定展开探究.
【查阅资料】
①制取漂白液的原理:Cl2+2NaOH═NaClO+NaCl+H2O,有效成分是NaClO;
②漂白液的漂白原理:NaClO在空气中很快发生反应:2NaClO+H2O+CO2═Na2CO3+2HClO,生成的HClO能使湿有色布条(含有机色素)褪色;
③HClO不稳定,易分解,分解后丧失漂白作用.
【提出问题】刚过期的漂白液是否失效?
【实验探究】该小组的实验报告如下:
小组同学对失效后漂白液的主要成分很感兴趣,纷纷提出猜想并作进一步探究.
【提出猜想】小立猜想:有NaCl
小英猜想:有NaCl、Na2CO3
小洁猜想:有NaCl、Na2CO3、NaOH
【设计方案】小组同学经过讨论,认为用足量的稀盐酸就可以验证小立的猜想是否成立.
为验证另两位同学的猜想,他们设计了如下方案:
最后,他们综合小组同学的设计,经实验得出了结论.
【查阅资料】
①制取漂白液的原理:Cl2+2NaOH═NaClO+NaCl+H2O,有效成分是NaClO;
②漂白液的漂白原理:NaClO在空气中很快发生反应:2NaClO+H2O+CO2═Na2CO3+2HClO,生成的HClO能使湿有色布条(含有机色素)褪色;
③HClO不稳定,易分解,分解后丧失漂白作用.
【提出问题】刚过期的漂白液是否失效?
【实验探究】该小组的实验报告如下:
| 实验操作 | 实验现象 | 实验结论 |
| 取适量该漂白液与烧杯中,放入有色布条 | 布条没有明显变化 | 该漂白液已完全失效 |
【提出猜想】小立猜想:有NaCl
小英猜想:有NaCl、Na2CO3
小洁猜想:有NaCl、Na2CO3、NaOH
【设计方案】小组同学经过讨论,认为用足量的稀盐酸就可以验证小立的猜想是否成立.
为验证另两位同学的猜想,他们设计了如下方案:
| 实验步骤 | 预期实验现象 | 实验目的或预期结论 |
| 步骤①;取少量该漂白液于试管中,加入足量CaCl2溶液,静置,观察 | 产生白色沉淀 | 目的:验证并除去Na2CO3 |
| 步骤②:取步骤①反应后上层清液于试管中,滴入无色酚酞试液,观察 | 试液变红 | 结论:小洁猜想成立猜想成立. |
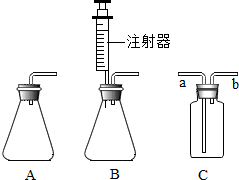 某化学小组同学用20%的过氧化氢溶液和二氧化锰,并选用A装置来制取氧气.
某化学小组同学用20%的过氧化氢溶液和二氧化锰,并选用A装置来制取氧气.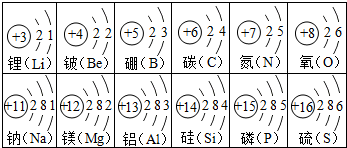 如图是部分元素的原子结构示意图,请回答:
如图是部分元素的原子结构示意图,请回答: