题目内容
2.硫氧二元素组成的化合物中,硫与氧二元素的质量之比为2:3,则该化合物的化学式及化合物中硫元素的化合价( )| A. | SO2 +4 | B. | SO+2 | C. | SO3 +6 | D. | 无法确定 |
分析 设出硫的氧化物的化学式,元素的质量等于该元素的相对原子质量×该元素的原子个数,根据硫元素与氧元素的质量比为2:3,计算出化学式中各元素的原子个数比,然后根据氧元素的化合价为-2价,以及化合物中各元素的化合价代数和为0进行解答.
解答 解:设硫的氧化物化学式为:SXOY根据:$\frac{32X}{16Y}$=$\frac{2}{3}$,解得X:Y=1:3,则硫的氧化物的化学式可表示为SO3;
设化合物中S元素化学价为x,已知O元素为-2价,依据化合物中各元素的化合价代数和为0的原则,有x+(-2)×3=0,解得x=+6;
故选C.
点评 要学会根据元素质量比书写化学式的方法以及求元素的化合价,关键是知道元素的质量等于该元素的相对原子质量×该元素的原子个数.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
17.下列化学方程式书写正确的是( )
| A. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2↑+2H2O | B. | H2+CuO═Cu+CO2 | ||
| C. | 2HgO $\frac{\underline{\;加热\;}}{\;}$2Hg+O2↑ | D. | 2CuO+C $\frac{\underline{\;高温\;}}{\;}$Cu+CO2 |

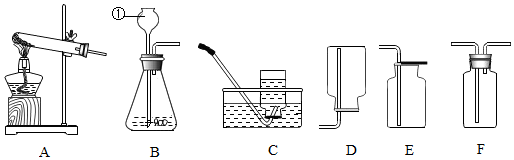
 为了比较人体呼出的气体和吸入的空气中二氧化碳含量的高低,某同学设计了图中所示的装置.
为了比较人体呼出的气体和吸入的空气中二氧化碳含量的高低,某同学设计了图中所示的装置.