题目内容
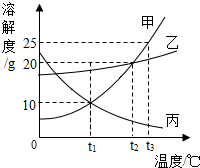 如图甲、乙、丙三种物质的溶解度曲线.据图回答:
如图甲、乙、丙三种物质的溶解度曲线.据图回答:(1)t3℃时,甲、乙、丙三种物质的溶解度关系是
(2)t2℃时将等质量三种物质的饱和溶液升温至t3℃,其溶液的质量关系是
(3)甲物质中含有少量的乙,要提纯甲通常采用的方法是
(4)将20克甲物质完全溶解于100克水中,不能形成饱和溶液的温度范围是
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用
专题:溶液、浊液与溶解度
分析:(1)根据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(2)根据三种物质的溶解度随温度变化情况即饱和溶液中溶质的质量分数计算方法分析解答;
(3)根据甲物质的溶解度受温度的影响考虑;
(4)根据将20克甲物质完全溶解于100克水中形成饱和溶液的温度范围来考虑.
(2)根据三种物质的溶解度随温度变化情况即饱和溶液中溶质的质量分数计算方法分析解答;
(3)根据甲物质的溶解度受温度的影响考虑;
(4)根据将20克甲物质完全溶解于100克水中形成饱和溶液的温度范围来考虑.
解答:解:
(1)根据溶解度曲线可知:t3℃时,甲、乙、丙三种物质的溶解度大小关系为 甲>乙>丙;
(2)由图可知:甲乙的溶解度在t2℃时相等,且二者的溶解度随温度的升高而增大,所以把t2℃时等质量的三种物质的饱和溶液升高温度至t3℃,甲乙无溶质析出,溶质的质量分数不变,丙的 溶解度随温度升高而减小,所以升温丙析出晶体,溶质的质量分数减小;饱和时质量分数的计算公式
×100%,即溶解度越大质量分数也就越大,据图可知:t2℃时甲乙的溶解度大于t3℃时丙的溶解度,所以升温后三种溶液的溶质质量分数大小关系是甲=乙>丙;
(3)由于甲物质的溶解度受温度影响很大,所以甲中含有少量一时,通常采用冷却热饱和溶液(即降温结晶)的方法,提纯甲;
(4)由于20克甲物质完全溶解于100克水中恰好达到饱和时,说明该温度时它的溶解度是20g,通过曲线图可知t2℃甲的溶解度为20g,小于这一温度,溶解度也小于20g,都属于饱和状态,大于这一温度时,溶解度大于20g,这时就属于不饱和状态了.
答案:
(1)甲>乙>丙 (2)甲=乙>丙 (3)降温结晶 (4)大于t2
(1)根据溶解度曲线可知:t3℃时,甲、乙、丙三种物质的溶解度大小关系为 甲>乙>丙;
(2)由图可知:甲乙的溶解度在t2℃时相等,且二者的溶解度随温度的升高而增大,所以把t2℃时等质量的三种物质的饱和溶液升高温度至t3℃,甲乙无溶质析出,溶质的质量分数不变,丙的 溶解度随温度升高而减小,所以升温丙析出晶体,溶质的质量分数减小;饱和时质量分数的计算公式
| 溶解度 |
| 溶解度+100g |
(3)由于甲物质的溶解度受温度影响很大,所以甲中含有少量一时,通常采用冷却热饱和溶液(即降温结晶)的方法,提纯甲;
(4)由于20克甲物质完全溶解于100克水中恰好达到饱和时,说明该温度时它的溶解度是20g,通过曲线图可知t2℃甲的溶解度为20g,小于这一温度,溶解度也小于20g,都属于饱和状态,大于这一温度时,溶解度大于20g,这时就属于不饱和状态了.
答案:
(1)甲>乙>丙 (2)甲=乙>丙 (3)降温结晶 (4)大于t2
点评:本题主要考查了学生对溶解度曲线意义的掌握和溶质的质量分数计算,掌握相关知识才能正确解答.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
《舌尖上的中国》是中央电视台播出的美食类纪录片,2014年4月18日起播出第二季,主要内容为中国各地美食生态.厨房是制作美食的主要场地,下列在厨房发生的变化中,不属于化学变化的是( )
A、 苹果腐烂 |
B、 榨取果汁 |
C、 面包发霉 |
D、 菜刀生锈 |
将下列各组物质同时加入到足量水中,最终能得到无色、透明溶液的是( )
| A、BaCl2、NaOH、H2SO4 |
| B、KNO3、NaCl、CuSO4 |
| C、HCl、Na2CO3、K2SO4 |
| D、KMnO4、Na2SO4、KCl |
 体育中考时很多同学从药店购买葡萄糖注射液,想在长跑前给自己补充能量和体液.为测定葡萄糖注射液的溶质质量分数与标签所示是否相符(见图),化学兴趣小组的同学采用了如下方法:取50g该注射液于烧杯中,逐滴滴加新制的氢氧化铜并加热,至不再产生沉淀为止,经过滤、洗涤、干燥后,称量固体质量为2.0g.该反应原理为:C6H12O6+2Cu(OH)2
体育中考时很多同学从药店购买葡萄糖注射液,想在长跑前给自己补充能量和体液.为测定葡萄糖注射液的溶质质量分数与标签所示是否相符(见图),化学兴趣小组的同学采用了如下方法:取50g该注射液于烧杯中,逐滴滴加新制的氢氧化铜并加热,至不再产生沉淀为止,经过滤、洗涤、干燥后,称量固体质量为2.0g.该反应原理为:C6H12O6+2Cu(OH)2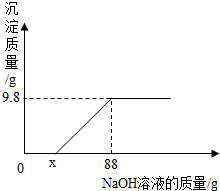 在绵阳市2014实验操作考试结束后,同学们在帮助老师整理实验室时,对酸性硫酸铜溶液(含有硫酸)产生了兴趣,在经老师允许后他们经行了如下的探究,取一定量的酸性硫酸铜溶液,向混合溶液中逐滴加入10%的氢氧化钠溶液,记录了如图所示的曲线关系.请根据曲线关系完成以下问题:
在绵阳市2014实验操作考试结束后,同学们在帮助老师整理实验室时,对酸性硫酸铜溶液(含有硫酸)产生了兴趣,在经老师允许后他们经行了如下的探究,取一定量的酸性硫酸铜溶液,向混合溶液中逐滴加入10%的氢氧化钠溶液,记录了如图所示的曲线关系.请根据曲线关系完成以下问题: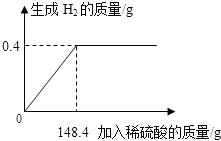 向16克黄铜(铜-锌合金)样品中加入稀硫酸使其充分反应,经实验测得所加稀硫酸与生成气体的质量关系如图所示.
向16克黄铜(铜-锌合金)样品中加入稀硫酸使其充分反应,经实验测得所加稀硫酸与生成气体的质量关系如图所示.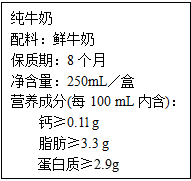 人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体(Ca5(PO4)3(OH))形式存在,其相对分子质量为502.牛奶含钙丰富又易被吸收,且牛奶中钙和磷比例合适,是健骨的理想食品.如图是某乳业公司纯牛奶包装标签的部分说明.请仔细阅读后回答下列问题:
人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体(Ca5(PO4)3(OH))形式存在,其相对分子质量为502.牛奶含钙丰富又易被吸收,且牛奶中钙和磷比例合适,是健骨的理想食品.如图是某乳业公司纯牛奶包装标签的部分说明.请仔细阅读后回答下列问题: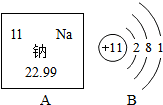 如图中A是钠元素在元素周期表中的相关信息,B是钠原子结构示意图.
如图中A是钠元素在元素周期表中的相关信息,B是钠原子结构示意图.