题目内容
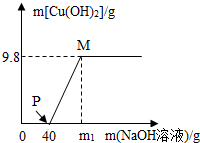 向含CuCl2和HCl的100g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图. 据图回答:
向含CuCl2和HCl的100g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图. 据图回答:(1)整个反应过程中,溶液中
(2)P点溶液中的溶质是
(3)M点溶液中的溶质质量分数是多少?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据复分解反应的实质生成沉淀 气体或水时离子数目减少,没参与反应的离子数目不变分析;
(2)根据整个反应过程的生成物及反应物来判断;
(3)M点溶液中的溶质是氯化钠,氯化钠有两部分,一是盐酸与氢氧化钠生成的,另一部分是氯化铜和氢氧化钠反应生成的;溶液质量可用质量守恒法来求,加入的混合溶液的总质量+氢氧化钠溶液的质量-生成的氢氧化铜沉淀的质量.从而求出溶液中溶质质量分数.
(2)根据整个反应过程的生成物及反应物来判断;
(3)M点溶液中的溶质是氯化钠,氯化钠有两部分,一是盐酸与氢氧化钠生成的,另一部分是氯化铜和氢氧化钠反应生成的;溶液质量可用质量守恒法来求,加入的混合溶液的总质量+氢氧化钠溶液的质量-生成的氢氧化铜沉淀的质量.从而求出溶液中溶质质量分数.
解答:解:(1)CuCl2和HCl的混合溶液中,逐滴加入NaOH溶液,氯化氢先与氢氧化钠反应生成氯化钠和水,然后氯化铜再与氢氧化钠反应生成氢氧化铜沉淀和氯化钠,化学方程式为:NaOH+HCl═NaCl+H2O;CuCl2+2NaOH═Cu(OH)2↓+2NaCl,由化学方程式可以看出,在此整个过程中,氯离子不变,其符号为:Cl-.
(2)P点表示氯化氢和氢氧化钠恰好完全反应,此时氯化铜还没和氢氧化钠反应,故溶液中的溶质为NaCl CuCl2;(3)设生成9.8g氢氧化铜沉淀需氢氧化钠溶液的质量为x,生成氯化钠的质量为z
CuCl2+2NaOH═Cu(OH)2↓+2NaCl,
80 98 117
x?10% 9.8g z
=
=
x=80g z=11.7g
氯化氢和氢氧化钠反应时消耗的氢氧化钠溶液的质量为40g,所以m1=40g+80g=120g
设氯化氢与氢氧化钠反应生成氯化钠的质量为y
NaOH+HCl═NaCl+H2O
40 58.5
40×10%=4g y
=
解得:y=5.85g
M点溶液中的溶质氯化钠的质量为11.7g+5.85g=17.55g
M点溶液的溶质质量分数=
×100%=8.35%
答:M点溶液的溶质质量分数为8.34%.
(2)P点表示氯化氢和氢氧化钠恰好完全反应,此时氯化铜还没和氢氧化钠反应,故溶液中的溶质为NaCl CuCl2;(3)设生成9.8g氢氧化铜沉淀需氢氧化钠溶液的质量为x,生成氯化钠的质量为z
CuCl2+2NaOH═Cu(OH)2↓+2NaCl,
80 98 117
x?10% 9.8g z
| 80 |
| x?10% |
| 98 |
| 9.8g |
| 117 |
| z |
x=80g z=11.7g
氯化氢和氢氧化钠反应时消耗的氢氧化钠溶液的质量为40g,所以m1=40g+80g=120g
设氯化氢与氢氧化钠反应生成氯化钠的质量为y
NaOH+HCl═NaCl+H2O
40 58.5
40×10%=4g y
| 40 |
| 4g |
| 58.5 |
| y |
解得:y=5.85g
M点溶液中的溶质氯化钠的质量为11.7g+5.85g=17.55g
M点溶液的溶质质量分数=
| 17.55g |
| 100g+120g-9.8g |
答:M点溶液的溶质质量分数为8.34%.
点评:本题考查化学方程式与溶液的综合计算,解题关键是分析清楚反应过程的先后,找出每个过程中已知物质的质量.

练习册系列答案
 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案
相关题目
在一定条件下,下列物质间的转化不能一步实现的是( )
| A、CO2→O2 |
| B、S→SO3 |
| C、CuSO4→Cu |
| D、Na2CO3→NaOH |
区分日常生活中的下列各组物质,所用方法不正确的是( )
| 选项 | 需区分的物质 | 实验方法 |
| A | 白酒和白醋 | 闻气味 |
| B | 食盐和白糖 | 加稀盐酸 |
| C | 锦纶和蚕丝 | 点燃闻气味 |
| D | 软水和硬水 | 加肥皂水 |
| A、A | B、B | C、C | D、D |
下列物质不属于氧化物的是( )
| A、二氧化碳 | B、二氧化硫 |
| C、氧化铝 | D、氧气 |
下列物质由离子构成的是( )
| A、汞 | B、氮气 |
| C、氯化钠 | D、二氧化碳 |