题目内容
3.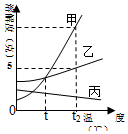 如图是甲、乙、丙三种固体的溶解度曲线,回答下列问题:
如图是甲、乙、丙三种固体的溶解度曲线,回答下列问题:(1)如果想配制同温度下的甲、乙两种溶液的饱和溶液,应该将温度控制在t1℃;
(2)t2℃时,向50克水中加入50克乙物质,充分溶解,所得溶液的质量分数33.3%;(保留0.1%)
(3)t1℃甲、乙、丙的饱和溶液升温到t2℃,所得溶液中溶质质量分数的大小关系为甲=乙>丙;(填“>”、“<”或“=”);
(4)若固体乙中含有少量的甲,可用蒸发结晶方法提纯乙(填“蒸发结晶”或“降温结晶”).
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)据图可以看出,要想配制同温度下的甲、乙两种溶液的饱和溶液,应该将温度控制在t1℃,故填:t1;
(2)t2℃时,乙的溶解度为50g,故向50克水中加入50克乙物质,充分溶解,只能溶解25g,故所得溶液的质量分数为:$\frac{25g}{25g+50g}×100%≈33.3%$,故填:33.3%;
(3)t1℃甲、乙、丙的饱和溶液升温到t2℃,甲和乙的溶液组成不变,而丙会析出固体,故所得溶液中溶质质量分数的大小关系为甲=乙>丙,故填:甲=乙>丙;
(4)乙的溶解度随温度的升高变化不大,故固体乙中含有少量的甲,可用蒸发结晶的方法提纯乙,故填:蒸发结晶.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案
相关题目
13.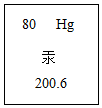 如图是汞元素在元素周期表中的相关信息,下列说法正确的是( )
如图是汞元素在元素周期表中的相关信息,下列说法正确的是( )
 如图是汞元素在元素周期表中的相关信息,下列说法正确的是( )
如图是汞元素在元素周期表中的相关信息,下列说法正确的是( )| A. | 汞是非金属元素 | B. | 贡原子核外电子数是80 | ||
| C. | 汞原子的质量是200.6 | D. | 汞原子核内有80个中子 |
14.下列反应类型判断错误的是( )
| 选项 | 化学方程式 | 反应类型 |
| A | 2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl | 化合反应 |
| B | Cu(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑ | 分解反应 |
| C | C2H3OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O | 置换反应 |
| D | Ca(OH)2+H2SO4═2H2O+CaSO4 | 复分解么应 |
| A. | A | B. | B | C. | C | D. | D |
11.下面是初中化学教材中出现的化学反应,对现象描述错误的是( )
| A. | 铁丝在氧气中燃烧生成黑色固体 | |
| B. | 石蕊试液可以使氨水变蓝色 | |
| C. | 向澄清的石灰水中通入二氧化碳气体,会观察到白色不溶物出现 | |
| D. | 硫磺在空气中燃烧发出淡蓝色火焰 |
18.下表中除去物质中少量杂质的方法正确的是( )
| 选项 | 物质(括号内为杂质) | 除杂试剂 |
| A | C(CuO) | 盐酸 |
| B | CaCl2溶液(HCl ) | Ba(OH)2溶液 |
| C | CO(CO2) | 碱石灰(CaO和NaOH混合物) |
| D | NaOH溶液(Ca(OH)2) | NaNO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
15.下列对部分化学知识的归纳完全正确的一组是( )
| A | 化学与生活:①生活中常用加热煮沸的方法软化硬水 ②氧气用于医疗急救 ③农业上用石灰乳和硫酸铜制波尔多液 |
| B | 化学与环境:①焚烧植物秸秆不会造成空气污染 ②PM2.5是造成雾霾天气的元凶之一 ③使用可降解塑料可减少“白色污染” |
| C | 化学与安全:①皮肤沾上浓硫酸--先用水冲洗,再涂稀醋酸 ②实验时碰倒酒精灯着火--用湿抹布盖灭 ③冬天用煤炉取暖--保证室内通风 |
| D | 化学与健康:①人体缺铁会引起贫血症 ②可用硫磺熏蒸笋干使之颜色更好看 ③制作糕点过程中加入适量的碳酸氢钠,使糕点松软可口 |
| A. | A | B. | B | C. | C | D. | D |
16.某石油化工厂化验室的实验员用20%的氢氧化钠溶液洗涤一定量石油产品中的残余稀硫酸,测得实验数据如表:
请回答下列问题:
(1)欲计算出一定量石油产品中所含H2SO4的质量,你觉得应该选择实验序号②的数据.
(2)当PH>7时,溶液中的溶质是硫酸钠和氢氧化钠
(3)若一定量石油产品中残余稀硫酸的质量为100g,请计算该残余稀硫酸的溶质质量分数.(写 出详细的计算过程)
| 实验序号 | 消耗NaOH溶液的质量 | 洗涤后溶液的pH |
| ① | 30g | pH<7 |
| ② | 40g | pH=7 |
| ③ | 50g | pH>7 |
(1)欲计算出一定量石油产品中所含H2SO4的质量,你觉得应该选择实验序号②的数据.
(2)当PH>7时,溶液中的溶质是硫酸钠和氢氧化钠
(3)若一定量石油产品中残余稀硫酸的质量为100g,请计算该残余稀硫酸的溶质质量分数.(写 出详细的计算过程)
 震惊全国的“三鹿奶粉”事件中的罪魁祸首是三聚氰胺(分子结构如图),三剧情三是一种重要的化工原料,由于其含氮量高,且目前国际上又通用“测氮法”标定牛奶中蛋白质含量,于是一些不法商人就将其混入奶粉中以“提高”奶粉的品质.
震惊全国的“三鹿奶粉”事件中的罪魁祸首是三聚氰胺(分子结构如图),三剧情三是一种重要的化工原料,由于其含氮量高,且目前国际上又通用“测氮法”标定牛奶中蛋白质含量,于是一些不法商人就将其混入奶粉中以“提高”奶粉的品质.