题目内容
10.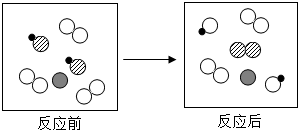 如图表示发生某化学反应前、后的微观示意图,根据图示请回答:
如图表示发生某化学反应前、后的微观示意图,根据图示请回答:(1)反应前容器中有1种单质分子;
(2)参加反应的各反应物的分子个数比为1:2;
(3)由“
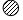 ”构成的物质不一定(填“一定”、“不一定”或、“一定不”)是该反应的催化剂;
”构成的物质不一定(填“一定”、“不一定”或、“一定不”)是该反应的催化剂;(4)反应前后没有变化的粒子有关③④⑤⑥(填序号)
①
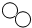 ②
②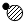 ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧
分析 根据微粒的构成分析物质的类别,根据微粒的变化分析分子、原子的变化,参加反应的各反应物的分子个数比等.
解答 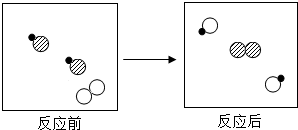 解:由微粒的变化可知,各物质反应的微粒个数关系是:
解:由微粒的变化可知,各物质反应的微粒个数关系是:
(1)由微粒的构成可知,反应前容器中有1种单质分子;
(2)由上图可知,参加反应的各反应物的分子个数比为1:2;
(3)由“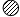 ”构成的物质不一定是该反应的催化剂;
”构成的物质不一定是该反应的催化剂;
(4)反应前后没有变化的粒子是原子,表示原子的图示有③④⑤⑥.
故答案为:(1)1;(2)1:2;(3)不一定;(4)③④⑤⑥.
点评 利用反应微观图中各物质分子的结构图,准确判断分子构成是解决问题的基础和重要手段.

练习册系列答案
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
1.下列关于“燃烧和灭火”的叙述正确的是( )
| A. | 室内起火时打开门窗通风 | |
| B. | 炒菜时油锅着火,立即盖上锅盖 | |
| C. | 只有含碳元素的物质才能燃烧 | |
| D. | 只要温度达到着火点,可燃物就能燃烧 |
18.质量守恒定律是化学反应乃至自然界最基本的定律之一,依据质量守恒定律我们可以精确的定量研究化学反应.最早传播和用文字记载并使人们普遍接受质量守恒定律的科学家是( )
| A. |  门捷列夫 门捷列夫 | B. |  达尔文 达尔文 | ||
| C. |  拉瓦锡 拉瓦锡 | D. |  牛顿 牛顿 |
5.在反应2A+B=3C+D中,A和B的相时分子质量之比为5:1,己知20gA与一定量B恰好完全反应,生成5gD,则在此反应中B和C的质量比为( )
| A. | 6:17 | B. | 2:17 | C. | 4:19 | D. | 1:3 |
15.下表中除杂方法正确的是( )
| 选项 | 物质 | 所含杂质 | 除杂试剂或方法 |
| A | 二氧化碳 | 水蒸气 | 氢氧化钠固体 |
| B | 氧化铜 | 铜 | 加足量稀盐酸,过滤 |
| C | 氯化钠固体 | 泥沙 | 加水溶解、过滤、蒸发 |
| D | NaOH溶液 | Na2CO3 | 加入过量Ca(OH)2溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
2.下列反应的化学方程式书写正确的是( )
| A. | 碳酸的不稳定 H2CO3═CO2+H2O | |
| B. | 铝在氧气中燃烧 2Al+O2 $\frac{\underline{\;点燃\;}}{\;}$ Al2O3 | |
| C. | 乙醇在空气中燃烧 C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$ 2 CO2+3H2O | |
| D. | 铜与硝酸银溶液反应 Cu+AgNO3═CuNO3+Ag |
