题目内容
15.人体吸入的O2有2%转化为活性氧,它加速人体衰老,被称为“夺命杀手”,我国科学家尝试用Na2SeO3清除人体内的活性氧,关于Na2SeO3这种物质,下列说法正确的( )| A. | Na2SeO3属于氧化物 | |
| B. | Na2SeO3中Se的化合价为+4价 | |
| C. | Na2SeO3能清除体内活性氧是物理性质 | |
| D. | 保持Na2SeO3化学性质的最小微粒是原子 |
分析 A.根据氧化物的概念来分析;
B.根据化合物中元素化合价的计算方法来分析;
C.根据清除活性氧的原理来分析;
D.根据物质的结构来分析.
解答 解:A.氧化物是由两种元素组成的,而Na2SeO3是由三种元素组成的,故错误;
B.钠元素显+1价,氧元素显-2价,设硒元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×3=0,则x=+4价.故正确;
C.Na2SeO3能清除体内活性氧的过程是与活性氧发生化学反应生成Na2SeO4,属于化学性质,故错误;
D.Na2SeO3是由钠离子和亚硒酸根离子构成的,不是由原子直接构成的,所以保持其化学性质的微粒是钠离子和亚硒酸根离子,而不是原子,故错误.
故选B.
点评 本题考查了氧化物的概念、化合价的计算、物质的性质以及保持物质化学性质的粒子,难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
5.冰融化成水时,发生改变的是( )
| A. | 分子的种类 | B. | 分子间的间隔 | ||
| C. | 分子本身体积变大 | D. | 分子质量变小 |
3.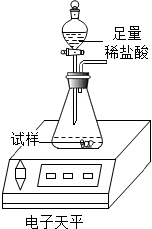 实验小组同学用如图所示装置测定某品牌食用纯碱的纯度,取该食用纯碱样品11.0g进行实验(样品中的杂质不与盐酸反应).实验数据记录如下(水和盐酸的挥发忽略不计):
实验小组同学用如图所示装置测定某品牌食用纯碱的纯度,取该食用纯碱样品11.0g进行实验(样品中的杂质不与盐酸反应).实验数据记录如下(水和盐酸的挥发忽略不计):
(1)反应生成CO2的质量为4.4g;
(2)计算该品牌食用纯碱中Na2CO3的质量分数.(写出计算过程,结果精确至0.1%)
 实验小组同学用如图所示装置测定某品牌食用纯碱的纯度,取该食用纯碱样品11.0g进行实验(样品中的杂质不与盐酸反应).实验数据记录如下(水和盐酸的挥发忽略不计):
实验小组同学用如图所示装置测定某品牌食用纯碱的纯度,取该食用纯碱样品11.0g进行实验(样品中的杂质不与盐酸反应).实验数据记录如下(水和盐酸的挥发忽略不计):| 时间/t | 0 | 20 | 30 | 40 |
| 装置+药品的质量/g | 171.0 | 167.0 | 166.6 | 166.6 |
(2)计算该品牌食用纯碱中Na2CO3的质量分数.(写出计算过程,结果精确至0.1%)
10.钙是人体必须的常量元素,为保持体内钙元素的量,青少年与中老年都需要“补钙”.如图是某钙片的部分说明书.请回答下列问题:
(1)写出该钙片中含有人体所需七大营养素中的两种钙元素和维生素.
(2)CaCO3中钙元素的质量分数为多大?
(3)若每片此钙片的质量为1g,按用量服用,每天摄入钙元素的质量为多少克?
| ×××钙片 [药品规格]每片含CaCO3 0.625g,维生素D100国际单位. [用法用量]每次1片,每天2次 |
(2)CaCO3中钙元素的质量分数为多大?
(3)若每片此钙片的质量为1g,按用量服用,每天摄入钙元素的质量为多少克?
20.有三瓶失去标签的无色溶液,已知分别是Na2SO4溶液、H2SO4溶液和Ca(NO3)2溶液中的各一种.下列四种试液中,能将上述三种无色溶液一次鉴别开来的是( )
| A. | 稀盐酸 | B. | BaCl2溶液 | C. | K2CO3溶液 | D. | 酚酞试液 |
4.推理是科学课学习中常见的思维方法.下列推理正确的是( )
| A. | 有机物都含有碳元素,所以含有碳元素的化合物一定是有机物 | |
| B. | 在同一化合物中,金属元素显正价,所以非金属元素一定显负价 | |
| C. | 某无色溶液,滴加紫色石蕊试液后,石蕊试液变蓝色,则该无色溶液的pH在13以上 | |
| D. | 铁与硫酸铜溶液、铜与硝酸银溶液、氢气和氧化铜之间都能发生置换反应,因此,置换反应不一定要在溶液中进行 |
2.推理是化学学习中常见的方法,下列推理正确的是( )
| A. | 有机物中均含碳元素,则含碳元素的化合物一定是有机物 | |
| B. | 单质由同种元素组成,则由同种元素组成的纯净物一定是单质 | |
| C. | 中和反应生成盐和水,则生成盐和水的反应一定是中和反应 | |
| D. | 活泼金属与稀硫酸反应产生气体,则与稀硫酸反应产生气体的物质一定是金属 |