题目内容
用如图微型仪器来完成制取并检验二氧化碳的实验只消耗了0.55g10%的盐酸(密度为1.1g/ml)。通过计算回答:
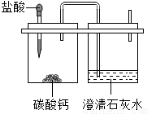
(1)产生二氧化碳的质量是多少?
(2)如果用锥形瓶来完成这个实验约需10%的盐酸5ml,
这是微型实验所用药品量的多少倍?
(1)0.03g (2)10
【解析】
试题分析:根据化学反应方程式:CaCO3+2HCl==CaCl2+H2O+CO2↑中HCl与CO2的质量关系,即可求出产生的二氧化碳质量
【解析】
设产生二氧化碳的质量为χ
0.55g10%的盐酸中含有溶质的质量为:0.55g×10% =0.055g
CaCO3+2HCl==CaCl2+H2O+CO2↑
73 44
0.055g χ
73/44 = 0.55g×10%/χ
χ = 0.03g
(2)0.55g10%盐酸的体积为:0.55g÷1.1g/ml =0.5ml
是微型实验所用药品量的倍数= 5ml/0.5ml =10
考点:根据化学方程式进行的计算

练习册系列答案
相关题目