题目内容
11.a、b两种物质的溶解度曲线如图所示.下列说法中,不正确的是( )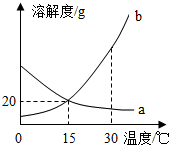
| A. | 15℃时,a、b的溶解度均为20 g | |
| B. | 加水或升温均可使b的饱和溶液变为不饱和溶液 | |
| C. | 将30℃时a的饱和溶液降温至15℃,溶质的质量分数不变 | |
| D. | 分别向100 g水中加入20 g a和b,升温至30℃,所得溶液均为饱和溶液 |
分析 根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小比较;
饱和溶液和不饱和溶液之间可以相互转化;
饱和溶液溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%;
根据物质的溶解度曲线、溶质质量、溶剂质量可以判断配制的溶液是否饱和.
解答 解:A、15℃时,a、b的溶解度均为20g,该选项说法正确;
B、b的溶解度随着温度升高而增大,因此加水或升温均可使b的饱和溶液变为不饱和溶液,该选项说法正确;
C、a的溶解度随着温度升高而减小,将30℃时a的饱和溶液降温至15℃时,变成不饱和溶液,溶质和溶剂质量都不变,因此溶质质量分数也不变,该选项说法正确;
D、30℃时,a的溶解度小于20g,b的溶解度大于20g,分别向100g水中加入20 ga和b,升温至30℃,a是饱和溶液,b是不饱和溶液,该选项说法不正确.
故选:D.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
2. 汞使用的历史很悠久,用途很广泛,在元素周期表中,汞元素的信息如图所示,对图中信息解释不正确的是( )
汞使用的历史很悠久,用途很广泛,在元素周期表中,汞元素的信息如图所示,对图中信息解释不正确的是( )
 汞使用的历史很悠久,用途很广泛,在元素周期表中,汞元素的信息如图所示,对图中信息解释不正确的是( )
汞使用的历史很悠久,用途很广泛,在元素周期表中,汞元素的信息如图所示,对图中信息解释不正确的是( )| A. | 汞原子核内质子数是80 | B. | 汞原子核外电子数是80 | ||
| C. | 汞属于非金属元素 | D. | 汞原子的相对原子质量是200.6 |
19. 实验室利用金属锌与稀硫酸反应制取氢气,另一种物质为硫酸锌.实验的相关数据如下表.
实验室利用金属锌与稀硫酸反应制取氢气,另一种物质为硫酸锌.实验的相关数据如下表.
(1)反应生成氢气的质量为0.4g(结果精确到0.1g,下同).
(2)计算参加反应的锌的质量,写出必要的计算过程.
 实验室利用金属锌与稀硫酸反应制取氢气,另一种物质为硫酸锌.实验的相关数据如下表.
实验室利用金属锌与稀硫酸反应制取氢气,另一种物质为硫酸锌.实验的相关数据如下表.| 气体发生装置内物质的总质量 | |
| 反应前 | 50g |
| 充分反应后 | 49.6g |
(2)计算参加反应的锌的质量,写出必要的计算过程.
6. 寿春中学化学组的同学设计了硫在氧气中燃烧的改良实验,如实验1.当火焰熄灭后发现留有剩余,硫为什么会熄灭呢?每个人都提出了自己的猜想.
寿春中学化学组的同学设计了硫在氧气中燃烧的改良实验,如实验1.当火焰熄灭后发现留有剩余,硫为什么会熄灭呢?每个人都提出了自己的猜想.
【猜想】
甲同学猜想:硫燃烧耗尽了瓶内的氧气,所以它熄灭了;
乙同学猜想:硫燃烧后瓶内的二氧化硫(不支持硫的燃烧)浓度过高导致硫熄灭了;
丙同学猜想:甲和乙都只看到了问题的一个方面,他认为甲和乙都有道理;
丁同学猜想:硫燃烧消耗氧气导致氧气浓度太低而熄灭.
【设计实验】丁同学设计了实验2进行实验验证自己的猜想:
【实验反思】(1)硫燃烧的化学方程式为S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;实验2中硫燃烧的火焰颜色是淡蓝色.
(2)实验1与课本实验相比,实验1的优点是避免SO2对大气污染;
(3)实验2中细沙的作用是防止红磷燃烧放出的热量使集气瓶炸裂.
(4)实验室中测定空气中氧气体积分数实验不用硫代替红磷的原因是硫燃烧生成气体使气压变化不明显.
 寿春中学化学组的同学设计了硫在氧气中燃烧的改良实验,如实验1.当火焰熄灭后发现留有剩余,硫为什么会熄灭呢?每个人都提出了自己的猜想.
寿春中学化学组的同学设计了硫在氧气中燃烧的改良实验,如实验1.当火焰熄灭后发现留有剩余,硫为什么会熄灭呢?每个人都提出了自己的猜想.【猜想】
甲同学猜想:硫燃烧耗尽了瓶内的氧气,所以它熄灭了;
乙同学猜想:硫燃烧后瓶内的二氧化硫(不支持硫的燃烧)浓度过高导致硫熄灭了;
丙同学猜想:甲和乙都只看到了问题的一个方面,他认为甲和乙都有道理;
丁同学猜想:硫燃烧消耗氧气导致氧气浓度太低而熄灭.
【设计实验】丁同学设计了实验2进行实验验证自己的猜想:
| 实验步骤 | 实验现象 | 实验分析 | 实验结论 |
| (1)把少量红磷放在铝制小盒内,然后放入装有细沙的集气瓶,塞紧瓶塞,用放大镜点燃硫,观察现象. | 硫燃烧一会儿就熄灭了. | 磷燃烧需满足的条件:①温度达到着火点; ②与氧气接触 | 丁同学的猜想正确. |
| (2)待冷却后,用放大镜聚光加热铝盒内的红磷,观察现象. | 红磷燃烧,放出热量的同时产生了白烟 |
(2)实验1与课本实验相比,实验1的优点是避免SO2对大气污染;
(3)实验2中细沙的作用是防止红磷燃烧放出的热量使集气瓶炸裂.
(4)实验室中测定空气中氧气体积分数实验不用硫代替红磷的原因是硫燃烧生成气体使气压变化不明显.
1.点燃下列各组物质,一定不会发生爆炸的是( )
| A. | 甲烷和空气 | B. | 二氧化碳和氧气 | C. | 面粉尘和空气 | D. | 氢气和氧气 |
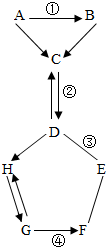 如图表示的是物质A-H相互间的关系(“→”表示物质间的转化关系,“-”表示两端的物质能发生化学反应).A、F都是单质,气体C常用于灭火,G是最轻的气体.请你回答:
如图表示的是物质A-H相互间的关系(“→”表示物质间的转化关系,“-”表示两端的物质能发生化学反应).A、F都是单质,气体C常用于灭火,G是最轻的气体.请你回答: 碳元素是组成许多物质的基本元素.
碳元素是组成许多物质的基本元素.