题目内容
13.钠元素对人类生命和生活具有重要意义.(1)钠元素广泛存在自然界中,亚硝酸钠(NaNO2)是一种常用的防腐剂,其中氮元素的化合价为+3;氯化钠在生活中常用于作调味品.
(2)叠氮化钠(NaN3)被广泛应用于汽车安全气囊,汽车经撞击后,30毫秒内引发NaN3迅速分解生成两种单质,写出反应的化学方程式2NaN3$\frac{\underline{\;撞击\;}}{\;}$2Na+3N2↑.
分析 (1)根据在化合物中正负化合价代数和为零、氯化钠的用途,进行分析解答.
(2)根据题意,汽车经撞击后,30毫秒内引发NaN3迅速分解生成两种单质,由质量守恒定律,反应前后元素的种类不变,两种单质是Na、N2,写出反应的化学方程式即可.
解答 解:(1)钠元素显+1价,氧元素显-2价,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(-2)×2=0,则x=+3价.
氯化钠在生活中常用于作调味品等.
(2)汽车经撞击后,30毫秒内引发NaN3迅速分解生成两种单质,由质量守恒定律,反应前后元素的种类不变,两种单质是Na、N2,反应的化学方程式为:2NaN3$\frac{\underline{\;撞击\;}}{\;}$2Na+3N2↑.
故答案为:(1)+3;作调味品等;(2)2NaN3$\frac{\underline{\;撞击\;}}{\;}$2Na+3N2↑.
点评 本题难度不大,掌握化合价的原则、氯化钠的用途、化学方程式的书写方法、质量守恒定律并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
3.下列推理正确的是( )
| A. | 化合物是由不同种元素组成的纯净物,所以由不同种元素组成的物质一定是化合物 | |
| B. | 碱溶液一定能使酚酞试剂变红,能使酚酞试剂变红的一定是碱溶液 | |
| C. | 分子、原子都是不带电的粒子,但是不带电的粒子不一定是分子、原子 | |
| D. | 中和反应一定有盐和水生成,所以有盐和水生成的反应一定是中和反应 |
8.勤劳的永兴人自古以来就学会了“银针验毒”的方法,其原理是:4Ag+2H2S+O2═2X+2H2O,X的化学式为( )
| A. | AgS | B. | Ag2O | C. | Ag2S | D. | Ag2O2 |
18.下列如图所示的实验设计中能达到目的是( )
| A. | 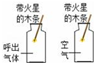 探究呼出气体和空气中氧气含量的不同 | |
| B. | 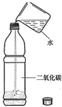 说明二氧化碳与水反应 | |
| C. | 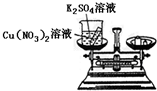 证明质量守恒定律 | |
| D. | 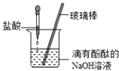 氢氧化钠能与盐酸反应 |
2.根据下列实验装置图,回答问题:
(1)写出图中标号仪器名称:a酒精灯、b长颈漏斗;
(2)实验室中若用装置A制取氧气,化学反应方程式为:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,若要收集一瓶较纯净的氧气,应选用的收集装置为C(填字母),若用该方法收集到的氧气中混有空气,可能的原因是导管口刚有气泡冒出时就收集了;
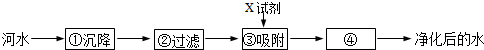
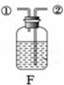
(3)实验室制取二氧化碳的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,可选择的发生装置和收集装置的组合为BD(填字母),检验二氧化碳是否集满的方法是将燃着的木条放在集气瓶口,若木条熄灭,证明已集满,用该方法制得的二氧化碳中常混有少量水蒸气,可用F装置除去,则F装置中应盛有的物质为浓硫酸,该混合气体应从F装置的②口(填“①”或“②”)通入.
| 发生装置 | 收集装置 | 洗气装置 |
 |  |  |
(2)实验室中若用装置A制取氧气,化学反应方程式为:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,若要收集一瓶较纯净的氧气,应选用的收集装置为C(填字母),若用该方法收集到的氧气中混有空气,可能的原因是导管口刚有气泡冒出时就收集了;
(3)实验室制取二氧化碳的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,可选择的发生装置和收集装置的组合为BD(填字母),检验二氧化碳是否集满的方法是将燃着的木条放在集气瓶口,若木条熄灭,证明已集满,用该方法制得的二氧化碳中常混有少量水蒸气,可用F装置除去,则F装置中应盛有的物质为浓硫酸,该混合气体应从F装置的②口(填“①”或“②”)通入.
3.氢氧化铝是一种不溶于水的白色固体,能与稀盐酸反应,也能与氢氧化钠溶液反应.氢氧化铝与氢氧化钠溶液反应的化学方程式为:Al(OH)3+NaOH═NaAlO2+2H2O.下列有关说法错误的是( )
| A. | 向氯化铝溶液中逐滴加入氢氧化钠溶液,先产生白色沉淀,后来白色沉淀又消失 | |
| B. | 在NaAlO2中铝元素的化合价为+3价 | |
| C. | 向稀盐酸中加入氢氧化铝,发生中和反应 | |
| D. | 氢氧化铝属于氧化物 |