题目内容
 过氧化氢(俗名双氧水,化学式H2O2)既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.小明从试剂商店购得一瓶双氧水溶液,用于制取O2.其瓶上标签的部分文字如图所示,试解答下列问题:
过氧化氢(俗名双氧水,化学式H2O2)既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.小明从试剂商店购得一瓶双氧水溶液,用于制取O2.其瓶上标签的部分文字如图所示,试解答下列问题:(1)这瓶溶液可稀释为溶质质量分数为6%的溶液约
(2)根据化学方程式计算:这瓶溶液稀释后理论上可制得多少克氧气?
分析:(1)根据溶液中溶质相等的关系,进行分析解答本题;
根据标签上的说明文字避光,低温密封保存,推测双氧水具有的性质;
(2)根据双氧水制取O2的化学方程式进行计算.
根据标签上的说明文字避光,低温密封保存,推测双氧水具有的性质;
(2)根据双氧水制取O2的化学方程式进行计算.
解答:解:(1)设 这瓶溶液可稀释为溶质质量分数为6%的溶液约 mg,
m×6%=500g×10%,
解答m=833.3g;
根据标签上的说明文字避光,低温密封保存,推测双氧水具有的性质为:见光、受热易分解;
故答案为:833.3; 见光、受热易分解;
(2)解:设生成的氧气质量为x,据题意得
2H2O2
2H2O+O2↑
68 32
500×10%克 x克
∴
=
解之得:x=23.5克
答:这瓶溶液稀释后理论上可制得23.5克氧气.
m×6%=500g×10%,
解答m=833.3g;
根据标签上的说明文字避光,低温密封保存,推测双氧水具有的性质为:见光、受热易分解;
故答案为:833.3; 见光、受热易分解;
(2)解:设生成的氧气质量为x,据题意得
2H2O2
| ||
68 32
500×10%克 x克
∴
| 68 |
| 500×10%克 |
| 32 |
| x克 |
解之得:x=23.5克
答:这瓶溶液稀释后理论上可制得23.5克氧气.
点评:本题主要考查化学方程式的书写和有关化学方程式的计算,及溶液与溶质的关系.

练习册系列答案
相关题目
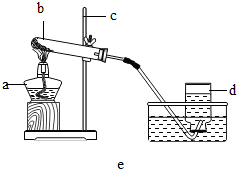 实验室可用如下两种方法制取氧气
实验室可用如下两种方法制取氧气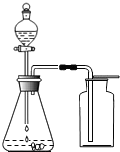
 过氧化氢(俗名双氧水,化学式H2O2)既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.小明从试剂商店购得一瓶双氧水溶液,用于制取O2.其瓶上标签的部分文字如图所示,试解答下列问题:
过氧化氢(俗名双氧水,化学式H2O2)既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.小明从试剂商店购得一瓶双氧水溶液,用于制取O2.其瓶上标签的部分文字如图所示,试解答下列问题: 实验室可用如下两种方法制取氧气
实验室可用如下两种方法制取氧气
