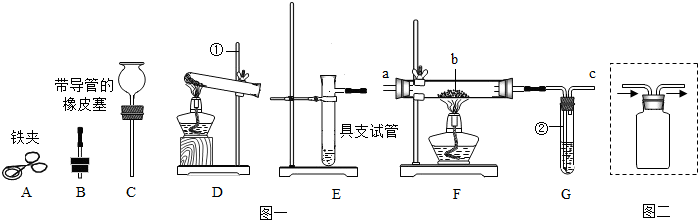
题目内容
利用废铁屑与一定质量分数的稀硫酸反应制取硫酸亚铁.现有80g废铁屑与430mL20%的稀硫酸(密度为1.14g/cm3)恰好完全反应(假设废铁屑中除铁以外的物质不溶于水且不与稀硫酸反应).我能完成下列计算(结果保留整数):(1)稀硫酸中溶质的质量;
(2)废铁屑中铁的质量;
(3)恰好完全反应时所得溶液中溶质的质量分数.
【答案】分析:由于废铁屑中除铁以外的物质不溶于水且不与稀硫酸反应,因此废铁屑与稀硫酸恰好完全反应所得溶液为硫酸亚铁溶液;根据反应的化学方程式,由所使用稀硫酸中硫酸的质量,计算出参加反应铁的质量、反应生成硫酸亚铁的质量及放出氢气质量,可完成废铁屑中铁的质量及恰好完全反应时所得溶液中溶质的质量分数的计算.
解答:解:(1)硫酸中溶质的质量:1.14g/cm3×430mL×20%=98g
(2)设80g废铁屑中铁的质量为x,生成硫酸亚铁的质量为y,生成氢气的质量为z.
Fe+H2SO4═FeSO4+H2↑
56 98 152 2
x 98g y z
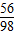 =
=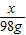 x=56g
x=56g
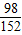 =
=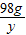 y=152g
y=152g
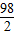 =
=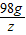 z=2g
z=2g
(3)所得溶液中溶质的质量分数: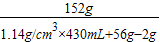 ×100%≈28%
×100%≈28%
答:(1)稀硫酸中溶质的质量是98g;(2)废铁屑中铁的质量为56g;(3)恰好完全反应时所得溶液中溶质的质量分数为28%.
点评:根据质量守恒定律,恰好完全反应后所得溶液的质量=参加反应铁的质量+所加稀硫酸的质量-反应放出氢气的质量.
解答:解:(1)硫酸中溶质的质量:1.14g/cm3×430mL×20%=98g
(2)设80g废铁屑中铁的质量为x,生成硫酸亚铁的质量为y,生成氢气的质量为z.
Fe+H2SO4═FeSO4+H2↑
56 98 152 2
x 98g y z
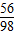 =
=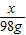 x=56g
x=56g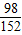 =
=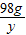 y=152g
y=152g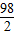 =
=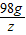 z=2g
z=2g(3)所得溶液中溶质的质量分数:
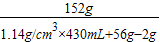 ×100%≈28%
×100%≈28%答:(1)稀硫酸中溶质的质量是98g;(2)废铁屑中铁的质量为56g;(3)恰好完全反应时所得溶液中溶质的质量分数为28%.
点评:根据质量守恒定律,恰好完全反应后所得溶液的质量=参加反应铁的质量+所加稀硫酸的质量-反应放出氢气的质量.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目