题目内容
7.通过海水晒制可得粗盐,粗盐中除NaCl外,还含有MgCl2、CaCl2、MgSO4以及泥沙等杂质.以下是一种由粗盐制备精盐的实验方案流程图:
分析该流程图,回答下列问题:
(1)试剂X为Na2CO3(填写化学式).
(2)加适量HCl溶液的目的是除去过量NaOH溶液和过量Na2CO3溶液.
(3)操作Y蒸发结晶.
(4)选择除杂的试剂不能用KOH代替NaOH溶液,理由是会引入新杂质KCl.
分析 粗盐中的MgCl2、CaCl2、Na2SO4都溶于水,要想将杂质除去必须将MgCl2、CaCl2和Na2SO4转化为沉淀,连同泥沙一起过滤除去.
解答 解:本实验的过程为;①粗盐提纯的第一步是溶解,搅拌时要用到玻璃棒,以加快粗盐溶解.
②加入过量BaCl2溶液,与Na2SO4发生反应,生成BaSO4沉淀和NaCl;
③加过量NaOH溶液,与MgCl2发生反应,生成Mg(OH)2沉淀和氯化钠;
④加过量Na2CO3溶液,与CaCl2和①中过量BaCl2溶液发生反应,生成CaCO3沉淀和BaCO3沉淀和氯化钠;
⑤过滤,滤出前面生成的沉淀及泥沙;
⑥加适量盐酸,与③中过量NaOH溶液和②中过量Na2CO3溶液发生反应,生成氯化钠、水和二氧化碳气体.
⑦氯化钠溶液蒸发、结晶,得到精盐.
故答案为:
(1)Na2CO3
(2)除去过量NaOH溶液和过量Na2CO3溶液
(3)蒸发结晶
(4)会引入新杂质KCl
点评 本题主要考查了粗盐提纯过程中的除杂方面的知识,综合性强,双基要求高.

练习册系列答案
相关题目
7.如表为某合金与铁的物理性质的比较,从性能上看,该合金不适合用作( )
| 熔点/℃ | 密度/(g/cm3) | 硬度(以金刚石的硬度为10作标准) | 异电性(以银的导电性为100作标准) | 耐腐蚀性 | |
| 某合金 | 2500 | 3.00 | 7.4 | 2.3 | 耐腐蚀 |
| 铁 | 1535 | 7.86 | 4.5 | 17 | 不耐腐蚀 |
| A. | 机械零件 | B. | 门窗 | C. | 保险丝 | D. | 飞机外壳 |
18.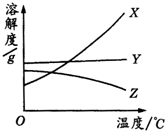 如图所示是X、Y、Z三种固体物质的溶解度曲线,当它们的溶液接近饱和时,分别采用增加溶质、蒸发溶剂、升高温度三种方法,均可以变成饱和溶液的是( )
如图所示是X、Y、Z三种固体物质的溶解度曲线,当它们的溶液接近饱和时,分别采用增加溶质、蒸发溶剂、升高温度三种方法,均可以变成饱和溶液的是( )
 如图所示是X、Y、Z三种固体物质的溶解度曲线,当它们的溶液接近饱和时,分别采用增加溶质、蒸发溶剂、升高温度三种方法,均可以变成饱和溶液的是( )
如图所示是X、Y、Z三种固体物质的溶解度曲线,当它们的溶液接近饱和时,分别采用增加溶质、蒸发溶剂、升高温度三种方法,均可以变成饱和溶液的是( )| A. | X溶液 | B. | Y溶液 | C. | Z溶液 | D. | X、Y溶液 |
15.推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 分子是构成物质的微粒,物质都是由分子构成的 | |
| B. | 氧化物一定含氧元素,含氧元素的物质一定是氧化物 | |
| C. | 碱性较强的溶液能使酚酞溶液变红,能使酚酞溶液变红的溶液一定呈碱性 | |
| D. | 中和反应生成盐和水,生成盐和水的反应一定是中和反应 |
12.某一份K2CO3样品中含Na2CO3、KNO3、Ba(NO3)2三种杂质中的一种或两种,把7.8g样品溶于足量水中得到澄清的溶液,再加足量CaCl2溶液,可得到5.0g沉淀,则原样品所含的杂质( )
| A. | 肯定有Na2CO3,没有Ba(NO3)2,可能有KNO3 | |
| B. | 肯定没有Na2CO3和KNO3,可能有Ba(NO3)2 | |
| C. | 肯定有KNO3,没有Ba(NO3)2,可能有Na2CO3 | |
| D. | 肯定有Na2CO3,肯定没有KNO3 |
16.M克食盐与N克水混合振荡,形成的溶液质量是( )
| A. | 一定等于(M+N)g | B. | 一定小于(M+N)g | C. | 等于或小于(M+N)g | D. | 无法判断 |

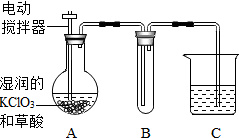 日前,世界环保联盟建议全面禁止用氯气对饮用水消毒,推广使用安全、高效杀菌消毒剂ClO2.①ClO2是一种黄绿色、有刺激性气味的气体,②冷却至11.0℃以下时变成红色液体,③易溶于水,④见光易分解,⑤易与碱反应,⑥杀菌、漂白能力均优于氯气.
日前,世界环保联盟建议全面禁止用氯气对饮用水消毒,推广使用安全、高效杀菌消毒剂ClO2.①ClO2是一种黄绿色、有刺激性气味的气体,②冷却至11.0℃以下时变成红色液体,③易溶于水,④见光易分解,⑤易与碱反应,⑥杀菌、漂白能力均优于氯气.