题目内容
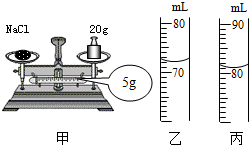
将图甲所示的托盘中的氯化钠全部倒入一洁净的烧杯中,再将图乙所示的量筒中的水全部倒入该烧杯中,搅拌,使其充分溶解.然后,将完全溶解后所得到的溶液全部倒入原量筒中,液面位置如图丙所示.则所得氯化钠溶液的密度为________g/cm3(精确到0.01),溶质的质量分数为________.(水的密度按1g/cm3计算)
1.20 25.8%
分析:根据托盘天平及量筒的使用方法,由图示读出溶质氯化钠的质量、水的体积及溶液的体积,利用溶液密度=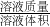 、溶液的溶质质量分数=
、溶液的溶质质量分数=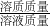 ×100%,完成计算.
×100%,完成计算.
解答:由托盘天平的示意图,所取氯化钠的质量为20g+5g=25g,所取水的体积为72mL合72g,所得溶液的体积为81mL;
则所得氯化钠溶液的密度=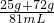 =1.20g/mL;溶质的质量分数=
=1.20g/mL;溶质的质量分数=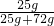 ×100%=25.8%
×100%=25.8%
故答案为:1.20;25.8%.
点评:通过操作图正确读出溶质质量与液体的体积是进行计算的基础,考查计量仪器的使用.
分析:根据托盘天平及量筒的使用方法,由图示读出溶质氯化钠的质量、水的体积及溶液的体积,利用溶液密度=
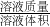 、溶液的溶质质量分数=
、溶液的溶质质量分数=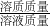 ×100%,完成计算.
×100%,完成计算.解答:由托盘天平的示意图,所取氯化钠的质量为20g+5g=25g,所取水的体积为72mL合72g,所得溶液的体积为81mL;
则所得氯化钠溶液的密度=
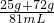 =1.20g/mL;溶质的质量分数=
=1.20g/mL;溶质的质量分数=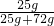 ×100%=25.8%
×100%=25.8%故答案为:1.20;25.8%.
点评:通过操作图正确读出溶质质量与液体的体积是进行计算的基础,考查计量仪器的使用.

练习册系列答案
 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
向一定量的硝酸银溶液中加入一定量的氯化钠溶液,充分反应后过滤,你认为滤液中溶质的组成最多有几种情况,根据你的猜想,选择一种可能的情况,设计下列实验方案进行探究,请将有关内容填写在下表中:
| 滤液中的溶质(一种猜想) | 验证的实验方法 | 可能观察到的实验现象 | 结论及化学方程式 |
我市某地盛产石灰石,其中含有不溶于盐酸的杂质.某化学兴趣小组用这种石灰石样品做制取二氧化碳的实验,取10.0g石灰石样品,经粉碎后全部放入烧杯中,并加入足量的稀盐酸,反应前烧杯及所盛物质的总质量为80.0g,其中烧杯质量为17.3g.反应过程中测得烧杯及所盛物质的质量与相应时间记录如下表:
| 反应时间/分 | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
| 烧杯及所盛物质质量/克 | 80.0 | 79.0 | 78.3 | 77.9 | 77.8 | m | 77.8 |
(1)表格中的m等于______.
(2)反应结束后,共收集二氧化碳______克的.
(3)完全反应后溶液中氯化钙的质量分数是多少?
 为了加快哈尔滨的经济发展,提高人民生活质量,市政府对哈市的路桥进行了大面积改造,下面认识正确的是
为了加快哈尔滨的经济发展,提高人民生活质量,市政府对哈市的路桥进行了大面积改造,下面认识正确的是