题目内容
某兴趣小组从废铝锅底部剪一块铝片,将它放入21.9%的稀盐酸中,产生氢气的质量与消耗盐酸的质量如下图(假设酸与氧化膜反应时没有H2产生,其他杂质不与酸反应)。请回答:
(1)从图中看出,该反应产生了H2________g。
(2)产生氢气的化学方程式为:________________________________________________________________________;铝片中铝单质的质量为________g。
(3)求被氧化的铝的质量占未氧化时铝片总质量的质量分数,写出计算过程。

(1)1.2 (2)2Al+6HCl===2AlCl3+3H2↑ 10.8
(3)解:设Al2O3的质量为x。
Al2O3+6HCl===2AlCl3+3H2O
102 6×36.5
x 50.0 g×21.9%
x=102×50.0 g×21.9%÷(6×36.5)=5.1 g
被氧化的铝的质量=5.1 g×2Al/Al2O3=5.1 g×(2×27/102)=2.7 g
被氧化的铝的质量占未氧化时铝片总质量的质量分数=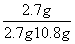 ×100%=20%
×100%=20%
解析:此题是图像型计算题,关键是抓特殊点“起点、终点、转折点”,同时要知道“废铝锅底部这一块铝片”表面是Al2O3,因此起点的50.0 g就是与Al2O3反应的稀盐酸质量。“求被氧化的铝的质量占未氧化时铝片总质量的质量分数”时,应将Al2O3质量换算成铝的质量。

练习册系列答案
相关题目
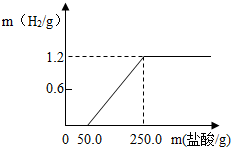 某兴趣小组从废铝锅底部剪一块铝片,将它放入21.9%的稀盐酸中,产生氢气的质量与消耗盐酸的质量如图所示(假设酸与氧化膜反应时没有H2产生,其它杂质不与酸反应),请回答:
某兴趣小组从废铝锅底部剪一块铝片,将它放入21.9%的稀盐酸中,产生氢气的质量与消耗盐酸的质量如图所示(假设酸与氧化膜反应时没有H2产生,其它杂质不与酸反应),请回答:
