题目内容
5.下列属于纯净物的是( )| A. | 井水 | B. | 空气 | C. | 氧气 | D. | 海水 |
分析 本题考查利用纯净物的概念来判断物质是否为纯净物,宏观上看只有一种物质,微观上只有一种分子.
解答 解:A、井水中含有钙镁化合物、水等物质,属于混合物,故A错;
B、空气中含有氧气、氮气、二氧化碳等物质,属于混合物,故B错;
C、氧气是由一种物质组成,属于纯净物,故C正确;
D、海水中含有氯化钠、氯化镁、水等物质,属于混合物,故D错.
故选C.
点评 在熟悉概念的基础上能从宏观和微观两个方面来判断纯净物和混合物,还要从社会实践中了解生活中常见物质的组成.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
18.若R元素无可变化化合价,其氯化物的化学式为RCl3,则下列化学式正确的是( )
| A. | RO | B. | R(NO3)3 | C. | R2(SO4)3 | D. | ROH |
20.下列关于实验现象的描述错误的是( )
| A. | 石灰石与稀盐酸混合后白色固体表面产生大量二氧化碳气体 | |
| B. | 硫酸铜溶液与氢氧化钠溶液混合溶液中产生蓝色絮状沉淀 | |
| C. | 蜡烛燃烧放出热量 | |
| D. | 向装有人呼出气体的集气瓶中滴入几滴澄清石灰水,澄清石灰水变白色浑浊 |
17.一名同学要用托盘天平称量12.5克的食盐固体,他在称量过程中发现指针向右偏转,此时应该( )
| A. | 减少砝码 | B. | 移动游码 | C. | 增加食盐 | D. | 减少食盐 |
14.下列实验操作正确的是( )
| A. |  取固体药品 | B. | 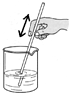 固体溶解 | C. | 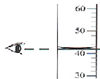 读取液体的体积 | D. | 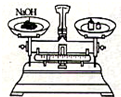 称量固体质量 |
15.实验室中有一瓶烧碱固体,打开瓶盖在空气中一段时间后,小王认为它可能变质,请你和他一起探究.
(1)小王认为烧碱暴露在空气中会变质的原因是:2NaOH+CO2═Na2CO3+H2O(写化学方程式),所以保存氢氧化钠必须密封.
(2)小王认为这瓶烧碱的可能组成有:A、全部是烧碱;B、全部是碳酸钠;小李认为还有第三种可能性,请你说出是烧碱和碳酸钠.
(3)对于第三种可能性,小李设计了一下的探究实验,请你帮他一起完成:
(4)请你写出上面第二步的化学方程式:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
(5)你认为小李的第二步设计正确吗?说出理由不正确,因为氢氧化钙溶液显碱性,过量的氢氧化钙溶液能使酚酞试液变红色;再有氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,氢氧化钠能使酚酞试液变红色.
(6)除上面用到的检验固体中含有碳酸钠的方法外,请你用另外一种不同类别的物质检验固体中含有碳酸钠,这种试剂是氯化钙,反应的化学方程式CaCl2+Na2CO3═CaCO3↓+2NaCl.
(7)小赵认为检验固体中有氢氧化钠的实验可以这样设计:取少量固体,加水充分溶解,往其中滴加酚酞试剂,变红色,呈碱性,说明固体中还有氢氧化钠.这种设计合理吗?说明理由不合理,因为碳酸钠溶液也显碱性,即使固体中没有氢氧化钠,溶液也能使酚酞试液变红色.
(1)小王认为烧碱暴露在空气中会变质的原因是:2NaOH+CO2═Na2CO3+H2O(写化学方程式),所以保存氢氧化钠必须密封.
(2)小王认为这瓶烧碱的可能组成有:A、全部是烧碱;B、全部是碳酸钠;小李认为还有第三种可能性,请你说出是烧碱和碳酸钠.
(3)对于第三种可能性,小李设计了一下的探究实验,请你帮他一起完成:
| 实验步骤 | 现象 | 结论 |
| 1.取少量固体,往其中滴加稀盐酸. | 有气泡冒出 | 固体中含有碳酸钠 |
| 2、另取少量固体,加水充分溶解,加入过量的氢氧化钙溶液. | 产生白色沉淀 | 固体中含有碳酸钠. |
| 3、对上述反应后的混合物过滤,在滤液中加入酚酞溶液. | 变红色 | 固体中含有氢氧化钠. |
(5)你认为小李的第二步设计正确吗?说出理由不正确,因为氢氧化钙溶液显碱性,过量的氢氧化钙溶液能使酚酞试液变红色;再有氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,氢氧化钠能使酚酞试液变红色.
(6)除上面用到的检验固体中含有碳酸钠的方法外,请你用另外一种不同类别的物质检验固体中含有碳酸钠,这种试剂是氯化钙,反应的化学方程式CaCl2+Na2CO3═CaCO3↓+2NaCl.
(7)小赵认为检验固体中有氢氧化钠的实验可以这样设计:取少量固体,加水充分溶解,往其中滴加酚酞试剂,变红色,呈碱性,说明固体中还有氢氧化钠.这种设计合理吗?说明理由不合理,因为碳酸钠溶液也显碱性,即使固体中没有氢氧化钠,溶液也能使酚酞试液变红色.
 实验室有一瓶浓硫酸,瓶上标签内容如图所示,请你根据标签上提供的数据解答下列问题.
实验室有一瓶浓硫酸,瓶上标签内容如图所示,请你根据标签上提供的数据解答下列问题.