题目内容
20.20℃时氯化钠的溶解度是36g,则氯化钠属于( )| A. | 易溶物质 | B. | 可溶物质 | C. | 微溶物质 | D. | 难溶物质 |
分析 物质的溶解性是根据在20℃(室温)时的溶解度来划分的,溶解度大于10g,属于易溶物质;溶解度大于1g,属于可溶物质;溶解度在0.01g~1g之间的,属于微溶物质;小于0.01g的,属于难溶物质(习惯上叫不溶);据此进行分析判断.
解答 解:物质的溶解性是根据在20℃(室温)时的溶解度来划分的,由题意20℃时氯化钠的溶解度是36g,溶解度大于10g,属于易溶物质.
A、20℃时氯化钠的溶解度是36g,大于10g,则氯化钠属于易溶物质,故选项正确.
B、20℃时氯化钠的溶解度是36g,大于10g,则氯化钠属于易溶物质,不属于可溶物质,故选项错误.
C、20℃时氯化钠的溶解度是36g,大于10g,则氯化钠属于易溶物质,不属于微溶物质,故选项错误.
D、20℃时氯化钠的溶解度是36g,大于10g,则氯化钠属于易溶物质,不属于难溶物质,故选项错误.
故选:A.
点评 本题难度不大,熟悉固体物质溶解性的分类与分类依据(室温时的溶解度)是正确解答本题的关键.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
10.实验废液中可能含有离子K+、Mg2+、Cl-、Ba2+、SO42-、CO32-中的几种,为确定可能含有的离子,兴趣小组进行了下面的实验:
①取一份废液,加入氯化钡溶液有白色沉淀产生,再加入足量稀盐酸,沉淀无变化;
②另取一份废液,加入氢氧化钾溶液出现白色沉淀,再加入足量稀盐酸,沉淀全部溶解.
分析上面实验得出的结论中,正确的是( )
①取一份废液,加入氯化钡溶液有白色沉淀产生,再加入足量稀盐酸,沉淀无变化;
②另取一份废液,加入氢氧化钾溶液出现白色沉淀,再加入足量稀盐酸,沉淀全部溶解.
分析上面实验得出的结论中,正确的是( )
| A. | 只含有Mg2+、SO42- | |
| B. | 一定含有Cl-、K+,可能含有Mg2+、SO42- | |
| C. | 一定含有Mg2+、SO42-,可能含有Cl-、K+ | |
| D. | 一定含有K+、Mg2+、Cl-、SO42- |
11.下列化学用语与含义相符的是( )
| A. | 30-3个氧元素 | B. | SO3-1个三氧化硫分子 | ||
| C. | O3-3个氧原子 | D. | $\stackrel{+3}{Fe}$-1个铁离子 |
8.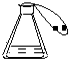 如图所示,将气球中的固体倒入锥形瓶中,气球将膨胀,则请你猜想,并填表(至少填两种):
如图所示,将气球中的固体倒入锥形瓶中,气球将膨胀,则请你猜想,并填表(至少填两种):
 如图所示,将气球中的固体倒入锥形瓶中,气球将膨胀,则请你猜想,并填表(至少填两种):
如图所示,将气球中的固体倒入锥形瓶中,气球将膨胀,则请你猜想,并填表(至少填两种):| 产生的气体 | 固体 | 液体 | 化学方程式 |
| 1 | |||
| 2 | |||
| 3 |
15.下列说法错误的是( )
| A. | 通常不指明溶剂的溶液,一般是指的是水溶液 | |
| B. | 50mL酒精与50mL水充分混合后可以得到100mL酒精溶液 | |
| C. | 食盐溶于水得到食盐水是化合反应 | |
| D. | 溶液中的溶质是以分子或离子的形式存在的 |
9.取硫酸溶液900g,平均分成6份,分别加入镁粉进行六次实验记录如下:
请将表中两个空格内的数据填上.
| 实验顺序 | 1 | 2 | 3 | 4 | 5 | 6 |
| 加入Mg质量(g) | 1 | 2 | 3 | 4 | 5 | 6 |
| MgSO4质量(g) | 5 | 10 | 15 | 18 | 18 | 18 |
10.生活中我们经常听说这些名词“加碘盐”、“补铁酱油”、“高钙奶”,这里的碘铁钙指的是( )
| A. | 元素 | B. | 原子 | C. | 分子 | D. | 单质 |