题目内容
10.超氧化钾(KO2)固体常用作氧气再生剂,主要作为潜艇、宇宙飞船舱的氧源或用于其他需要人工氧源的地方.用超氧化钾供氧时可发生如下反应:4KO2+□X═2K2CO3+3O2,其中X是一种常见气体.下列关于X的说法正确的是( )| A. | X由碳、氢、氧三种元素组成 | B. | 检验X用燃着的木条 | ||
| C. | X中碳、氧元素的质量比为3:4 | D. | X中碳、氧元素的化合价代数和为零 |
分析 根据反应方程式为4KO2+□X═2K2CO3+3O2,利用反应前后元素种类、原子个数和种类不变来推断X的化学式,进而根据化学式进行分析
解答 解:由反应方程式为4KO2+□X═2K2CO3+3O2,
根据质量守恒定律可知,
反应前后元素种类、原子个数和种类不变,
K原子个数前后相等,
反应后共2个C原子、12个O原子,
则反应前应共2个C原子、12个O原子,现有8个O原子,
即X中共含有2个C原子、4个O原子,
则X的化学式为CO2,X的化学计量数为2,故:
A、X不含氢元素,故错误;
B、二氧化碳用澄清的石灰水进行检验,故错误;
C、X中碳、氧元素的质量比为:12:(16×2)=3:8,故错误;
D、化合物中正负化合价代数和为零,故正确.
故选D.
点评 本题考查化学式的推断,学生应能利用原子守恒的方法来推导,将守恒思想这一学科思维方式贯穿在学习化学的过程中.

练习册系列答案
相关题目
20.下列对一些事实的解释中,不合理的是( )
| 选项 | 事实 | 解释 |
| A | 0.0151m3的钢瓶可以装入20m3的气体,但是只能装入0.015m3的水 | 气体分子之间有间隔,液态分子间没有间隔 |
| B | 将墨汁滴入一杯淸水中,清水很快变黑 | 分子在不断运动 |
| C | 1滴水的质量的为0.05g,大约含有1.67×l021个水分子 | 分子的质量和体积都很小 |
| D | 过氧化氢受热分解,水受热不分解 | 二者分子构成不同,分子是保持物质化学性质的最小微粒 |
| A. | A | B. | B | C. | C | D. | D |
1.下列除去杂质所用的药品或方法,正确的是( )
| 选项 | 物质 | 杂质 | 除杂药品或方法 |
| A | CO2 | CO | 灼热的铜网 |
| B | NaCl溶液 | MgCl2溶液 | 过量烧碱溶液,过滤 |
| C | 铁钉 | 铁锈 | 适量稀硫酸,洗涤、干燥 |
| D | 熟石灰 | 石灰石 | 高温煅烧 |
| A. | A | B. | B | C. | C | D. | D |
18.下列实验操作涉及化学变化的是( )
| A. |  过滤 | B. |  检验气体是否是氧气 | ||
| C. | 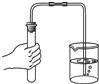 气密性检查 | D. | 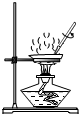 蒸发食盐水 |
5.小雨阅读课外资料得知:氯酸钾的分解可用二氧化锰、氧化铜等物质作催化剂.于是,他对影响过氧化氢分解的因素及催化剂的催化效果产生了探究兴趣.
【提出问题】氧化铜是否比二氧化锰催化效果更好?过氧化氢分解速率与哪些因素有关?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列几组实验.
(1)若t1>t2(填“>”、“=”、“<”),说明氧化铜能加快过氧化氢的分解速率.若要确定氧化铜是此反应的催化剂,还需探究反应前后,氧化铜的质量和化学性质不变.
(2)实验④中MnO2的质量为0.5g,若t3>t4,则化学反应快慢与温度的关系是温度越高,反应速率越快.
(3)写出实验④所涉及的化学方程式2H2O2$\frac{\underline{\;\;\;MnO_{2}\;\;\;}}{380℃}$2H2O+O2↑.
【得出结论】氧化铜能作过氧化氢分解的催化剂,且催化效果较好.
【评价设计】你认为小雨设计实验②和实验③对比的目的是比较氧化铜和二氧化锰的催化效果.
【拓展延伸】小雨想,除了催化剂外,影响过氧化氢溶液分解还有哪些因素呢?如果你能帮小雨提出合理的假设并设计方案
假设:
方案:
【提出问题】氧化铜是否比二氧化锰催化效果更好?过氧化氢分解速率与哪些因素有关?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列几组实验.
| 序号 | 5%过氧化氢溶液 | 其他物质 | 加热的温度 | 氧气的体积 | 反应所需时间 |
| ① | 2.0g | 330℃ | 100mL | t1 | |
| ② | 2.0g | CuO 0.5g | 330℃ | 100mL | t2 |
| ③ | 2.0g | MnO2 0.5g | 330℃ | 100mL | t3 |
| ④ | 2.0g | MnO20.5 g | 380℃ | 100mL | t4 |
(2)实验④中MnO2的质量为0.5g,若t3>t4,则化学反应快慢与温度的关系是温度越高,反应速率越快.
(3)写出实验④所涉及的化学方程式2H2O2$\frac{\underline{\;\;\;MnO_{2}\;\;\;}}{380℃}$2H2O+O2↑.
【得出结论】氧化铜能作过氧化氢分解的催化剂,且催化效果较好.
【评价设计】你认为小雨设计实验②和实验③对比的目的是比较氧化铜和二氧化锰的催化效果.
【拓展延伸】小雨想,除了催化剂外,影响过氧化氢溶液分解还有哪些因素呢?如果你能帮小雨提出合理的假设并设计方案
假设:
方案:
2.下列各组物质在pH=3的溶液中能大量共存,且形成无色溶液的是( )
| A. | KCl NaCl Na2CO3 | B. | AgNO3 NaNO3 HCl | ||
| C. | CuSO4 H2SO4 MgCl2 | D. | KNO3 Ca(NO3)2 NH4Cl |
19.下列关于四种粒子的结构示意图的说法中正确的是( )


| A. | ①③的化学性质相同 | |
| B. | ①属于离子,离子符号为Cl-1 | |
| C. | ①③属于同种元素 | |
| D. | ②表示的元素在化合物中通常显-1价 |
