题目内容
配平下列化学方程:
(1)________Al+________Fe3O4  ________Al2O3+________Fe
________Al2O3+________Fe
(2)________ NH3+________O2  ________NO+________H2O
________NO+________H2O
(3)________FeS2+________O2  ________Fe2O3+________SO2;
________Fe2O3+________SO2;
(4)________Fe2O3+________HCl=________FeCl3+________H2O.
 8;4;3;94;5;4;64;11;2;81;6;2;3
【解析】
(1)利用最小公倍数法进行配平,以氧原子作为配平的起点,Fe3O4、Al2O3前面的化学计量数分别为:3、4,最后调整铝、铁前面的化学计量数为8、9.(2)本题可利用“定一法”进行配平,把NH3的化学计量数定为1,则O2、NO、H2O前面的化学计量数分别为:、1、,同时扩大4倍,则NH3、O2、NO、H2O前面的化学...
8;4;3;94;5;4;64;11;2;81;6;2;3
【解析】
(1)利用最小公倍数法进行配平,以氧原子作为配平的起点,Fe3O4、Al2O3前面的化学计量数分别为:3、4,最后调整铝、铁前面的化学计量数为8、9.(2)本题可利用“定一法”进行配平,把NH3的化学计量数定为1,则O2、NO、H2O前面的化学计量数分别为:、1、,同时扩大4倍,则NH3、O2、NO、H2O前面的化学...
请用化学用语填空:
(1)天然气的主要成分是________;
(2)盐酸中溶质的成分是________。
 CH4 HCl
【解析】本题主要考查本题主要考查化学符号及其周围数字的意义。要分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式。
(1)天然气的主要成分甲烷,化学式为CH4,故填:CH4
(2)盐酸中溶质为氯化氢,化学式为HCl,故填:HCl
CH4 HCl
【解析】本题主要考查本题主要考查化学符号及其周围数字的意义。要分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式。
(1)天然气的主要成分甲烷,化学式为CH4,故填:CH4
(2)盐酸中溶质为氯化氢,化学式为HCl,故填:HCl 贝壳的主要成分是碳酸钙。为了测定某贝壳中碳酸钙的质量分数,小林同学进行了如下实验:将贝壳洗净、干燥并捣碎后,称取5 g 放在烧杯里,然后往烧杯中加入足量的稀盐酸45 g,充分反应后,称得反应剩余物为48.24 g。(假设其他物质不与盐酸反应)(1)产生二氧化碳气体 g。(2)计算该贝壳中碳酸钙的质量分数。
 1.76 80%
【解析】碳酸钙与稀盐酸反应! 生成氯化钙、水和二氧化碳:CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳是气体,会逸散到空气中,故烧杯中减少的质量即为生成的二氧化碳的质量。根据二氧化碳的质量,利用化学方程式,根据反应的质量比即可计算出贝壳中碳酸钙的质量。
生成的二氧化碳的质量=5g+45g-48.24g=1.76g
设5g贝壳中碳酸钙的质量为x;
...
1.76 80%
【解析】碳酸钙与稀盐酸反应! 生成氯化钙、水和二氧化碳:CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳是气体,会逸散到空气中,故烧杯中减少的质量即为生成的二氧化碳的质量。根据二氧化碳的质量,利用化学方程式,根据反应的质量比即可计算出贝壳中碳酸钙的质量。
生成的二氧化碳的质量=5g+45g-48.24g=1.76g
设5g贝壳中碳酸钙的质量为x;
... 下列关于水的蒸发过程,说法正确的是
A. 水分子之间间隔增大 B. 水分子体积增大
C. 水分子质量增加 D. 水分子个数增多
 A
【解析】
水蒸发是物理变化,分子的种类不变,分子间的间隔变大。故选A。
A
【解析】
水蒸发是物理变化,分子的种类不变,分子间的间隔变大。故选A。 《环境空气质量标准》中的PM2.5是指大气中直径小于或等于2.5微米的颗粒物。下列措施,能减少PM2.5污染的是
A. 提倡使用清洁能源 B. 提倡节日燃放烟花爆竹
C. 提倡多开私家车出行 D. 提倡大力发展煤炭火力发电
 A
【解析】
清洁能源包括太阳能、风能等,这些能源的使用不会产生PM2.5,A正确;
液化爆竹的燃放会产生大量的PM2.5,B错误;
汽车尾气中含有PM2.5,C错误;
煤炭燃烧除了会生成二氧化硫外,还会产生大量的PM2.5,D错误。
故选A。
A
【解析】
清洁能源包括太阳能、风能等,这些能源的使用不会产生PM2.5,A正确;
液化爆竹的燃放会产生大量的PM2.5,B错误;
汽车尾气中含有PM2.5,C错误;
煤炭燃烧除了会生成二氧化硫外,还会产生大量的PM2.5,D错误。
故选A。 配平下列化学方程式:
(1)________Al2O3 ________Al+________O2↑
________Al+________O2↑
(2)________C2H4+________O2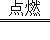 ________CO2+________H2O
________CO2+________H2O
(3)________KClO3 ________KCl+________O2↑
________KCl+________O2↑
(4)________Fe2O3+________CO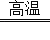 ________Fe+________CO2 .
________Fe+________CO2 .
 2; 4; 3; 1; 3; 2; 2; 2; 2; 3; 1; 3; 2; 3
【解析】
(1)利用最小公倍数法进行配平,以氧原子作为配平的起点,Al2O3、O2前面的化学计量数分别为:2、3,最后调整铝前面的化学计量数为4.
(2)本题可利用“定一法”进行配平,把C2H4的化学计量数定为1,则氧气、二氧化碳、水前面的化学计量数分别为:3、2、2.
(3)利用最小公倍数法...
2; 4; 3; 1; 3; 2; 2; 2; 2; 3; 1; 3; 2; 3
【解析】
(1)利用最小公倍数法进行配平,以氧原子作为配平的起点,Al2O3、O2前面的化学计量数分别为:2、3,最后调整铝前面的化学计量数为4.
(2)本题可利用“定一法”进行配平,把C2H4的化学计量数定为1,则氧气、二氧化碳、水前面的化学计量数分别为:3、2、2.
(3)利用最小公倍数法... 氢气在氧气中燃烧的化学方程式是:2H2+O2 2H2O,从这个化学方程式获得的信息错误的是
2H2O,从这个化学方程式获得的信息错误的是
A. 氢气与氧气在点燃的条件下生成水
B. 每2个氢分子与1个氧分子完全反应,生成2个水分子
C. 常温下,每2体积的氢气与l体积的氧气完全反应,生成2体积的水
D. 每4份质量的氢气与32份质量的氧气完全反应,生成36份质量的水
 C
【解析】
化学方程式能客观地反映出化学反应中“质”和“量”的变化及关系。化学方程式中的“+”号应读成“和”,不能读成“加”;反应物和生成物中间的“=”号,应读成“生成”,不能读成“等于”。A、氢气与氧气在点燃的条件下生成水,故A正确;B、每2个氢分子与1个氧分子完全反应,生成2个水分子,故B正确;C、常温下,不能说每2体积的氧气与l体积的氧气完全反应,生成2体积的水,物质状态不同,...
C
【解析】
化学方程式能客观地反映出化学反应中“质”和“量”的变化及关系。化学方程式中的“+”号应读成“和”,不能读成“加”;反应物和生成物中间的“=”号,应读成“生成”,不能读成“等于”。A、氢气与氧气在点燃的条件下生成水,故A正确;B、每2个氢分子与1个氧分子完全反应,生成2个水分子,故B正确;C、常温下,不能说每2体积的氧气与l体积的氧气完全反应,生成2体积的水,物质状态不同,... 下列实验操作错误的是( )
A. 倾倒液体时,取下的瓶盖倒放在桌面上
B. 倾倒液体时,标签向着手心
C. 加热时用手直接拿着试管
D. 实验时用剩的药品放到指定的容器(废液缸)
 C
【解析】
A、瓶塞正放在桌面上时,既污染了试剂,又腐蚀了桌面,所以取下的试剂瓶塞要倒放在桌子上,故说法正确;B、倒液体时,试剂瓶标签要正对手心,防止倾倒液体时,残留液腐蚀标签,故说法正确;C、加热时用试管夹加持试管,故说法错误;D、实验剩余的药品要放入指定容器内,故说法正确。故选C。
C
【解析】
A、瓶塞正放在桌面上时,既污染了试剂,又腐蚀了桌面,所以取下的试剂瓶塞要倒放在桌子上,故说法正确;B、倒液体时,试剂瓶标签要正对手心,防止倾倒液体时,残留液腐蚀标签,故说法正确;C、加热时用试管夹加持试管,故说法错误;D、实验剩余的药品要放入指定容器内,故说法正确。故选C。 某元素的原子结构示意图如图所示,其元素符号为Br。
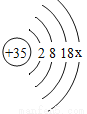
(1)其中x=________,Br属于________(填“金属”或“非金属”)元素。
(2)如图表示的微粒中包括________种元素的微粒;具有相对稳定结构的是________(填字母,下同),与Br化学性质相似的是________。
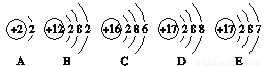
 7非金属4ADE
【解析】
(1)在原子中,核内质子数等于核外电子数,则x=35-2-8-18=7,故填7;该元素的原子最外层电子数为7,接近稳定结构,为非金属元素,故填非金属元素。
(2)决定元素种类的是原子核内的质子数可以判定这几种微粒属于四种元素,故填4;最外层电子数是8(或第一层为最外层且有2个电子)属于稳定结构,所以具稳定结构的是AD,故填AD;决定元素化学性质的是最外层电...
7非金属4ADE
【解析】
(1)在原子中,核内质子数等于核外电子数,则x=35-2-8-18=7,故填7;该元素的原子最外层电子数为7,接近稳定结构,为非金属元素,故填非金属元素。
(2)决定元素种类的是原子核内的质子数可以判定这几种微粒属于四种元素,故填4;最外层电子数是8(或第一层为最外层且有2个电子)属于稳定结构,所以具稳定结构的是AD,故填AD;决定元素化学性质的是最外层电... 
