题目内容
7. 如图是MgCl2、NaCl、MgSO4、KCl四种物质的溶解度曲线,请回答下列问题:
如图是MgCl2、NaCl、MgSO4、KCl四种物质的溶解度曲线,请回答下列问题:(1)20℃时,向两只盛有100g水的烧杯中,分别加入氯化钠、氯化镁两种物质,至不再溶解为止,所得溶液的溶质质量分数大的是氯化镁溶液;
(2)卤水(提取食盐后的母液)含有MgCl2、NaCl、MgSO4、KCl.其中镁盐占70%以上,现需从卤水中提取KCl固体,采用下列方法:
①将卤水加热蒸发水份就逐渐析出晶体A,滤出晶体得到母液R,根据右图所示溶解度曲线,晶体A中主要含有氯化钠,理由是氯化钠的溶解度随温度的变化不明显.
②将母液R降温(降到30℃以下)析出晶体B,则晶体B主要含有氯化钾,理由是氯化钾的溶解度随温度的降低而减小明显.
③将析出的晶体B,用一定量的冷水洗涤,就可以得到较纯的KCl固体,理由是氯化钾在冷水中的溶解度小.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)据图可以看出,20℃时,氯化镁的溶解度大,故向两只盛有100g水的烧杯中,分别加入氯化钠、氯化镁两种物质,至不再溶解为止,所得溶液的溶质质量分数大的是氯化镁溶液,故填:氯化镁;
(2)①因为氯化钠的溶解度随温度升高变化不明显,故将卤水加热蒸发水份就逐渐析出晶体A主要成分是氯化钠,故填:氯化钠;氯化钠的溶解度随温度的变化不明显.
②因为氯化钾的溶解度随温度的降低而减小明显,故将母液R降温(降到30℃以下)析出晶体B,则晶体B主要含有氯化钾,故填:氯化钾;氯化钾的溶解度随温度的降低而减小明显.
③氯化钾的溶解度在低温时小,故将析出的晶体B,用一定量的冷水洗涤,就可以得到较纯的KCl固体,故填:氯化钾在冷水中的溶解度小.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
17.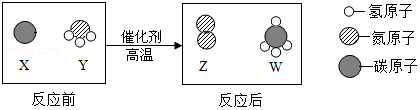 科学家最新发现,通过简单的化学反应,可以将树木纤维素转变成超级储能装置.如图是该反应的微观示意图,下列说法错误的是( )
科学家最新发现,通过简单的化学反应,可以将树木纤维素转变成超级储能装置.如图是该反应的微观示意图,下列说法错误的是( )
 科学家最新发现,通过简单的化学反应,可以将树木纤维素转变成超级储能装置.如图是该反应的微观示意图,下列说法错误的是( )
科学家最新发现,通过简单的化学反应,可以将树木纤维素转变成超级储能装置.如图是该反应的微观示意图,下列说法错误的是( )| A. | 该反应不属于置换反应 | |
| B. | 化学反应前后原子的种类、个数、质量均保持不变 | |
| C. | 参加反应的X、Y两物质的粒子个数比为3:4 | |
| D. | W物质中碳元素的质量分数为75% |
15.钛(Ti)和钛合金被认为是21世纪的重要金属材料.该化学方程式4NaH+X═Ti+4NaCl+2H2中X的化学式为( )
| A. | 2Cl2 | B. | HTi | C. | H2O | D. | TiCl4 |
2.胆矾是一种蓝色晶体,化学式是CuSO4•5H2O,胆矾受热时易失去结晶水,成为白色的无水CuSO4粉末,无水CuSO4易吸收水份又变成蓝色,在工业上精炼铜、镀铜等都要用胆矾.上述对胆矾的描述中,没有涉及到的是( )
| A. | 物理性质 | B. | 用途 | C. | 制法 | D. | 化学性质 |
19.有机物R和足量氧气置于密闭容器中充分反应生成水和二氧化碳,实验前后物质反应物质质量如表,下列说法错误的是( )
| R | O2 | CO2 | H2O | |
| 反应前物质质量/g | 46 | 128 | 0 | 0 |
| 反应后物质质量/g | 0 | 32 | X | 54 |
| A. | x=88 | B. | 参加反应质量比R:O2=23:64 | ||
| C. | R的化学式C2H5OH | D. | R是由C、H、O三种元素组成 |
20.下列图标中,属于回收标志的是( )
| A. |  | B. |  | C. |  | D. |  |
 北京八达岭太阳能热发电站的工作原理:通过集热塔上的吸热器吸收太阳能,将水加热成水蒸气推动汽轮机发电.
北京八达岭太阳能热发电站的工作原理:通过集热塔上的吸热器吸收太阳能,将水加热成水蒸气推动汽轮机发电.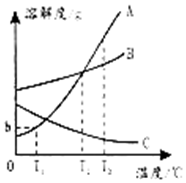 我国纪念2017年“世界水日”和“中国水周”活动的宣传主题为“落实绿色发展理念,全面推行河长制”.请回答下列与水有关的问题:
我国纪念2017年“世界水日”和“中国水周”活动的宣传主题为“落实绿色发展理念,全面推行河长制”.请回答下列与水有关的问题: