��Ŀ����
11�������ʷ������ϵ�У��ᡢ��κ��������Ƿdz���Ҫ�����������1����������������������ӹ��ɵģ���������ˮ��Һ��ˮ���ӵĴ���ʹ������ӷ����˽��룮������ӡ����������ˮ��Ҳ�ᷢ�����룬Ҳ���������һ�������H+�����û�ѧ�����ʾ����˺�������ᡢ����ʹ��ᶼ�й�ͬ�Ļ�ѧ���ʣ�
�������������;����������������������BC
A������������� B������ҩ���Ȼ�п C����ȥNaCl�е�����NaOH
��2���������Ƴ���¶���ڿ����У����ױ��ʣ�ԭ����2NaOH+CO2=Na2CO3+H2O���û�ѧ����ʽ��ʾ��
ʯ��ˮ����һЩ���ʷ�Ӧ���ٶ�����̼���Ȼ�þ��Һ��̼������Һ
���У�������������Һ����ʯ��ˮ��Ҳ��ͬ��������Ǣڣ���ţ���
��3���Ȼ��ƺ�̼���ƾ�����ܽ�ȣ�0�桫30�棩���±���ʾ��
| 0�� | 10�� | 20�� | 30�� | |
| NaCl��g�� | 35.7 | 35.8 | 36.0 | 36.3 |
| Na2CO3��g�� | 7.0 | 12.5 | 21.5 | 38.8 |
��������������õĴ�����������Ȼ��ƣ���ʵ���������������ִ�����Ʒ�����ⶨ��Ʒ�д����������������������ʵ�鲽�裮
a����ȡ10g������Ʒ�����ձ��У�
b�����ձ��м��������ij������Һ��������HNO3���÷�Ӧ�Ļ�ѧ����ʽ�ǣ�Na2CO3+2HNO3�T2NaNO3+H2O+CO2��
c���������ձ��м����������������Һ���۲쵽�а�ɫ�������÷�Ӧ��ѧ����ʽ�ǣ�AgNO3+NaCl�TAgCl��+NaNO3
d�����������ʵ�鲽���г���Ϊ0.287g������Ʒ��̼���Ƶ���������Ϊ��98.83%����ȷ��0.01%����
���� ��1����������ˮ��Һ�л����������ӣ����������������Ӳ�ͬ���з�����
��2�����ݶ�����̼���������Ʒ�Ӧ������̼���ƺ�ˮ���з�����
�����������ƺͶ�����̼��Ӧû�����������������Ʋ�����̼���Ʒ�Ӧ���з�����
��3���ٸ����Ȼ��ƺʹ�����ܽ�Ƚ��з�����
��b�����ݼ�������Ӱ���Ȼ��Ƶ��������������������ɳ������з�����
c�������Ȼ��ƺ��������������Ȼ��������������ƽ��з�����
d�����ݻ�ѧ����ʽ�����е����ݽ��м��㣮
��� �⣺��1������ˮ��Һ�л����������ӣ���ѧ����Ϊ��H+�����������������Ӳ�ͬ�����ܳ��⣬�����������ȡ�Ȼ�п�����ܳ�ȥ�������ƣ����������ʣ���ѡ��BC��
��2��������̼���������Ʒ�Ӧ������̼���ƺ�ˮ����ѧ����ʽΪ��2NaOH+CO2=Na2CO3+H2O��
�������ƺͶ�����̼��Ӧû�����������������Ʋ�����̼���Ʒ�Ӧ����ѡ���ڣ�
��3���ٸ����Ȼ��ƺʹ�����ܽ�Ƚ��з�����
��b����������Ӱ���Ȼ��Ƶ��������������������ɳ���������Ӧ�ü������ᣬ�����̼���Ʒ�Ӧ���������ơ�ˮ�Ͷ�����̼����ѧ����ʽΪ��Na2CO3+2HNO3�T2NaNO3+H2O+CO2����
c���Ȼ��ƺ��������������Ȼ��������������ƣ���ѧ����ʽΪ��AgNO3+NaCl�TAgCl��+NaNO3��
d����μӷ�Ӧ���Ȼ�������Ϊx
AgNO3+NaCl�TAgCl��+NaNO3
58.5 143.5
x 0.287g
$\frac{58.5}{x}$=$\frac{143.5}{0.287g}$
x=0.117g
������Ʒ��̼���Ƶ���������Ϊ��$\frac{10g-0.117g}{10g}$��100%=98.83%��
�ʴ�Ϊ����1��H+��BC��
��2��2NaOH+CO2=Na2CO3+H2O���ڣ�
��3���ٶ���
��b��HNO3��Na2CO3+2HNO3�T2NaNO3+H2O+CO2����
c��AgNO3+NaCl�TAgCl��+NaNO3��
d��98.83%��
���� �ڽ������ʱ�����ȷ������п�������⣬Ȼ�������е�֪ʶ��ѧ����֪ʶ���н��

 �������¿��ÿ�ʱ��ҵϵ�д�
�������¿��ÿ�ʱ��ҵϵ�д�| A�� |  ˮ�� ˮ�� | B�� |  ̫���� ̫���� | C�� |  ��ʯ��Դ ��ʯ��Դ | D�� |  ���� ���� |
| A�� | ��������ˮ | B�� | ���������� | ||
| C�� | ����ˮʱ���ų����� | D�� | ��Ӧ���Ű��� |
| A�� | ȼ��һ�㶼���淢��ͷ������������з���ͷ�������ı仯����ȼ�� | |
| B�� | ����R�ڿ�����ȼ��������ˮ�Ͷ�����̼������R��һ������̼���⡢��Ԫ�� | |
| C�� | ���ʯ��ʯī��C60����̼Ԫ����ɵĵ��ʣ����Խ��ʯ��ʯī��C60��ͬһ���� | |
| D�� | ij������ֻ����һ��Ԫ�أ�������һ�����ǻ����� |
| A�� | һЩԪ�ؿ����γɶ������� | |
| B�� | ������������ͬ��������ͬ��Ԫ�� | |
| C�� | ���Ԫ����ͬ�Ĵ����ﲻһ����ͬ������ | |
| D�� | Ԫ�صĻ�ѧ������ԭ�Ӻ���������������ϵ���� |
 ̼��̼�Ļ���������������������Ӧ�ù㷺�����ſƼ��ķ�չ����̼Ԫ�ص��²��ϲ���ӿ�֣��������ѧ֪ʶ�ش��������⣺
̼��̼�Ļ���������������������Ӧ�ù㷺�����ſƼ��ķ�չ����̼Ԫ�ص��²��ϲ���ӿ�֣��������ѧ֪ʶ�ش��������⣺
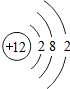 þԭ���ڻ�ѧ��Ӧ������ʧȥ����õ�����ʧȥ����2�����ӣ��γɵ����ӵķ�����Mg2+��þԪ�����ڽ�������������ǽ�������Ԫ�أ�
þԭ���ڻ�ѧ��Ӧ������ʧȥ����õ�����ʧȥ����2�����ӣ��γɵ����ӵķ�����Mg2+��þԪ�����ڽ�������������ǽ�������Ԫ�أ�