题目内容
如图是中学常见的实验装置图(图1)
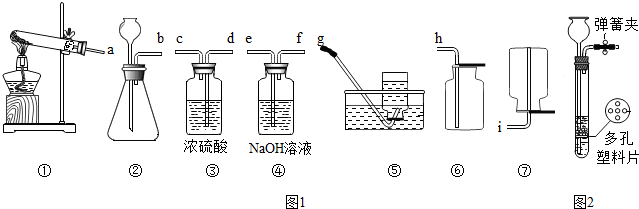
(1)实验室用锌粒和稀硫酸反应制取氢气,要制备并收集干燥的氢气,请将所选装置接口按从左到右顺序连接为 .
(2)实验室制取氧气有多种方法.
a.如用H2O2溶液制氧气其反应原理为 .如图2是实验室制备气体的一种装置图.该装置的特点是:打开弹簧夹,块状固体和液体接触,反应发生;关闭弹簧夹后,产生的气体将液面压回,使固体和液体分开,反应停止.用H2O2溶液制氧气时, (填“可以”或“不可以”)采用此装置.
b.实验室还用KClO3来制备氧气,该反应的化学方程式为 .将KClO3与MnO2的混合物ag加热一段时间,得到bg固体,将得到的固体溶于水,过滤、洗涤、干燥后,又得到cg固体,则KClO3的分解率为 .(用含a,b.c的式子表示)(提示:KClO3的分解率是指已分解KClO3质量与原加入KClO3质量之比.)
(3)实验室在常温下用块状电石(CaC2)与水反应制取微溶于水的乙炔(C2H2)气体.其反应的化学方程式为 该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂.你认为上图中最适合制取乙炔气体的发生装置需要做如何改进 .

(1)实验室用锌粒和稀硫酸反应制取氢气,要制备并收集干燥的氢气,请将所选装置接口按从左到右顺序连接为
(2)实验室制取氧气有多种方法.
a.如用H2O2溶液制氧气其反应原理为
b.实验室还用KClO3来制备氧气,该反应的化学方程式为
(3)实验室在常温下用块状电石(CaC2)与水反应制取微溶于水的乙炔(C2H2)气体.其反应的化学方程式为
考点:常用气体的发生装置和收集装置与选取方法,气体的干燥(除水),实验室制取氧气的反应原理,氢气的制取和检验,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)连接顺序的正确与否关系到收集的气体是否干燥、纯净;
(2)a、二氧化锰可以用作过氧化氢分解的催化剂,二氧化锰是一种粉末状固体;
b、氯酸钾在二氧化锰做催化剂、加热的条件下分解能生成氯化钾和氧气,根据提供的数据和反应的化学方程式可以计算氯酸钾的分解率.
(3)根据反应物和生成物即可写出有关反应的化学方程式;根据反应物的状态和反应的条件以及反应的特点,确定发生装置;据此解答.
(2)a、二氧化锰可以用作过氧化氢分解的催化剂,二氧化锰是一种粉末状固体;
b、氯酸钾在二氧化锰做催化剂、加热的条件下分解能生成氯化钾和氧气,根据提供的数据和反应的化学方程式可以计算氯酸钾的分解率.
(3)根据反应物和生成物即可写出有关反应的化学方程式;根据反应物的状态和反应的条件以及反应的特点,确定发生装置;据此解答.
解答:解:
(1)锌粒和稀硫酸反应制取氢气时不需要加热,可以选择②装置,干燥氢气时,应该用浓硫酸,氢气应该从d进入,从c出,因为氢气的密度比空气小,应该用向下排空气法收集,收集装置应该选择⑦,所以所选装置接口按从左到右顺序连接为:bdci.故填:bdci.
(2)a、用H2O2溶液制氧气其反应原理为2H2O2
2H2O+O2↑;过氧化氢分解可以选择二氧化锰做催化剂,二氧化锰是粉末状的,故用H2O2溶液制氧气时,不可以采用此装置.
b、在二氧化锰做催化剂、加热条件下,氯酸钾分解能生成氯化钾和氧气,
反应的化学方程式为:2KClO3
2KCl+3O2↑.
设反应的氯酸钾的质量为x,KClO3与MnO2的混合物ag加热一段时间,得到bg固体,生成氧气的质量是:(a-b)g,
2KClO3
2KCl+3O2↑,
245 96
x (a-b)g
则
=
,解得x=
g,过滤、洗涤、干燥后,又得到cg固体,cg固体是二氧化锰,
反应前氯酸钾的质量是:(a-c)g,KCl03的分解率为:
×100%,
(3)块状电石(CaC2)与水反应制取难溶于水的乙炔气体(C2H2)并生成了氢氧化钙,该反应的化学方程式是CaC2+2H2O═Ca(OH)2+C2H2↑;②换长颈漏斗,随时控制反应速率.
故答案为:
(1)bdci.
(2)a.2H2O2
2H2O+O2↑. 不可以.
b. 2KClO3
2KCl+3O2↑.
×100%.
(3)CaC2+2H2O═Ca(OH)2+C2H2↑,②换长颈漏斗.
(1)锌粒和稀硫酸反应制取氢气时不需要加热,可以选择②装置,干燥氢气时,应该用浓硫酸,氢气应该从d进入,从c出,因为氢气的密度比空气小,应该用向下排空气法收集,收集装置应该选择⑦,所以所选装置接口按从左到右顺序连接为:bdci.故填:bdci.
(2)a、用H2O2溶液制氧气其反应原理为2H2O2
| ||
b、在二氧化锰做催化剂、加热条件下,氯酸钾分解能生成氯化钾和氧气,
反应的化学方程式为:2KClO3
| ||
| △ |
设反应的氯酸钾的质量为x,KClO3与MnO2的混合物ag加热一段时间,得到bg固体,生成氧气的质量是:(a-b)g,
2KClO3
| ||
| △ |
245 96
x (a-b)g
则
| 245 |
| 96 |
| x |
| (a-b)g |
| 245(a-b) |
| 96 |
反应前氯酸钾的质量是:(a-c)g,KCl03的分解率为:
| 245(a-b) |
| 96(a-c) |
(3)块状电石(CaC2)与水反应制取难溶于水的乙炔气体(C2H2)并生成了氢氧化钙,该反应的化学方程式是CaC2+2H2O═Ca(OH)2+C2H2↑;②换长颈漏斗,随时控制反应速率.
故答案为:
(1)bdci.
(2)a.2H2O2
| ||
b. 2KClO3
| ||
| △ |
| 245(a-b) |
| 96(a-c) |
(3)CaC2+2H2O═Ca(OH)2+C2H2↑,②换长颈漏斗.
点评:本题考查了装置气密性检验、化学方程式的书写、计算等方面的知识,计算时一定要注意规范性和准确性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
原子失去最外层电子或在最外层得到电子后,不发生变化的是( )
①元素种类 ②化学性质 ③相对原子质量 ④粒子的电性
⑤原子核 ⑥电子数 ⑦最外层电子数.
①元素种类 ②化学性质 ③相对原子质量 ④粒子的电性
⑤原子核 ⑥电子数 ⑦最外层电子数.
| A、①③⑤ | B、②④⑥⑧ |
| C、②⑤ | D、①⑤ |