题目内容
请回答下列问题(在下列(1)(2)两小题中任选一题回答,若两小题都回答,则以第(1)小题的答案评定分数):(1)你知道无锡市政府所采取的防止太湖蓝藻爆发的措施有哪些?(至少两点)
(2)防治温室效应有哪些方法?(至少两点)
【答案】分析:本题是一道自选题,主要考查水污染和防治以及空气污染和防治的知识,要根据自己的选择,进行仔细分析,合理应答.
解答:解:若选(1),则从水污染的方面回答,水的主要污染来源有工业污染源、农业污染源、生活污染源,太湖蓝藻爆发是因为太湖水富营养化,就是含有的氮、磷元素过多造成的,今年爆发得晚,说明氮、磷的排放得到了有效的控制,采取的措施可能有禁止使用含磷洗衣粉,或湖区内要退耕还湖,或鼓励沿湖农民少用化肥,多用农家肥,或工业污水净化达标后再排放等.
故答案为:禁止使用含磷洗衣粉,或湖区内要退耕还湖,或鼓励沿湖农民少用化肥,多用农家肥,或工业污水净化达标后再排放等.
(2)导致温室效应的主要气体是二氧化碳,还有臭氧、甲烷、氟氯代烷等.可以采用减少使用化石燃料、开发使用清洁能源、植树造林等措施减少二氧化碳的排放.
故答案为:减少化石燃料的燃烧使用;使用清洁能源;植树造林等.
点评:本题考查的内容不太难,但设置的情景好,自选题的考查形式较灵活,能适应不同的学生,本题重在考查学生的环保意识,是对情感态度和价值观的考查.
解答:解:若选(1),则从水污染的方面回答,水的主要污染来源有工业污染源、农业污染源、生活污染源,太湖蓝藻爆发是因为太湖水富营养化,就是含有的氮、磷元素过多造成的,今年爆发得晚,说明氮、磷的排放得到了有效的控制,采取的措施可能有禁止使用含磷洗衣粉,或湖区内要退耕还湖,或鼓励沿湖农民少用化肥,多用农家肥,或工业污水净化达标后再排放等.
故答案为:禁止使用含磷洗衣粉,或湖区内要退耕还湖,或鼓励沿湖农民少用化肥,多用农家肥,或工业污水净化达标后再排放等.
(2)导致温室效应的主要气体是二氧化碳,还有臭氧、甲烷、氟氯代烷等.可以采用减少使用化石燃料、开发使用清洁能源、植树造林等措施减少二氧化碳的排放.
故答案为:减少化石燃料的燃烧使用;使用清洁能源;植树造林等.
点评:本题考查的内容不太难,但设置的情景好,自选题的考查形式较灵活,能适应不同的学生,本题重在考查学生的环保意识,是对情感态度和价值观的考查.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
乙醇(C2H5OH)是以高梁、玉米、薯类等为原料,经过发酵、蒸馏制得,属于可再生资源.乙醇在足量的氧气中完全燃烧时生成二氧化碳和水,如果氧气不足,乙醇燃烧可能还有一氧化碳生成.现用下图实验装置进行实验,检验乙醇的燃烧产物中是否有二氧化碳和一氧化碳:(友情提示:CO+CuO
CO2+Cu)

请回答下列问题:
(1)写出乙醇在足量的氧气中完全燃烧的化学方程式 .
(2)有甲、乙、丙三个同学分别完成上述实验并将观察到的现象填写在下表中,试用“有”、“没有”和“可能有”填写下表中的实验结论.
(3)若燃烧一定量的乙醇,得到了4.4g二氧化碳和5.6g一氧化碳,在该反应过程中生成水的质量是 .
| ||

请回答下列问题:
(1)写出乙醇在足量的氧气中完全燃烧的化学方程式
(2)有甲、乙、丙三个同学分别完成上述实验并将观察到的现象填写在下表中,试用“有”、“没有”和“可能有”填写下表中的实验结论.
| 实验现象 | 实验结论 | ||||
| A装置 | C装置 | E装置 | 是否有二氧化碳 | 是否有一氧化碳 | |
| 甲同学 | 石灰水 变浑浊 |
石灰水 没变浑浊 |
石灰水 没变浑浊 |
||
| 乙同学 | 石灰水 变浑浊 |
石灰水 变浑浊 |
石灰水 变浑浊 |
||
| 丙同学 | 石灰水 没变浑浊 |
石灰水 没变浑浊 |
石灰水 变浑浊 |
||
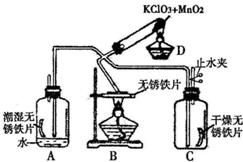 33、为了验证铁与氧气在不同条件下的反应情况,设计如图所示(部分铁架台已略去)的实验,D装置是O2发生装置,A为铁在有水存在下与O2反应装置,B为无锈铁片在加热条件下与O2反应装置,C装置是验证在干燥条件下O2与铁反应装置(C装置事先干燥过).请回答下列问题:
33、为了验证铁与氧气在不同条件下的反应情况,设计如图所示(部分铁架台已略去)的实验,D装置是O2发生装置,A为铁在有水存在下与O2反应装置,B为无锈铁片在加热条件下与O2反应装置,C装置是验证在干燥条件下O2与铁反应装置(C装置事先干燥过).请回答下列问题:
 (2013?荆门)某化学兴趣小组使用右图所示装置,对某种铁铜合金的成分进行测量.先取足量稀硫酸于烧杯中,再向其中加入14.0g合金样品开始计时,并将电子天平的读数记录在下表中,请回答下列问题:
(2013?荆门)某化学兴趣小组使用右图所示装置,对某种铁铜合金的成分进行测量.先取足量稀硫酸于烧杯中,再向其中加入14.0g合金样品开始计时,并将电子天平的读数记录在下表中,请回答下列问题: