题目内容
18.用化学符号或化学式来表示.(1)5个二氧化碳分子5CO2,
(2)镁元素Mg,
(3)2个铁原子2Fe,
(4)空气中含量最多的气体N2,
(5)2个钠离子2Na+,
(6)负二价的硫酸根离子$\stackrel{-2}{S{O}_{4}}$.
(7)氢氧化铝Al(OH)3,
(8)硝酸钙Ca(NO3)2,
(9)硫酸铝Al2(SO4)3,
(10)氯化亚铁FeCl2,
(11)2个氢分子2H2,
(12)碳酸钾K2CO3,
(13)氧化铜CuO,
(14)4个碳酸根离子4CO32-,
(15)3个硝酸分子3HNO3.
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:(1)根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,因此5个二氧化碳分子表示为:5CO2;
(2)元素用元素符号表示,因此镁元素表示为:Mg;
(3)原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.所以2个铁原子,就可表示为2Fe;
(4)空气中含量最多的气体是氮气,氮气是双原子分子构成的气体,所以氮气的化学式就是在氮元素的元素符号下写一个2,即:N2;
(5)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故2个钠离子可表示为:2Na+.
(6)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素(或原子团)的上方用正负号和数字表示,正负号在前,数字在后,所以负二价的硫酸根离子表示为:$\stackrel{-2}{S{O}_{4}}$;
(7)氢氧化铝中氢氧根的化合价是-1价,铝元素显+3价,根据化合价原则其化学式是Al(OH)3;
(8)硝酸钙是由显+2价的钙元素和显-1价的硝酸根组成的,根据化合价原则其化学式是Ca(NO3)2;
(9)硫酸铝是由显+3价的铝元素和显-2价的硫酸根组成的,根据化合价原则其化学式是Al2(SO4)3;
(10)氯化亚铁是由+2价的铁元素和显-1价的氯元素组成的,根据化合价原则其化学式是FeCl2;
(11)根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,因此2个氢分子表示为:2H2;
(12)碳酸钾是由显+1价的钾元素和显-2价的碳酸根组成的,根据化合价原则其化学式是K2CO3;
(13)氧化铜是由+2价的铜元素和显-2价的氧元素组成的,根据化合价原则其化学式是CuO;
(14)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.表示多个离子在离子符号前面加数字,故4个碳酸根离子符号为:4CO32-;
(15)正确书写物质的化学式,氢元素显+1价,硝酸根显-1价,根据化合价原则,硝酸可表示为:HNO3;
故答案为:(1)5CO2;(2)Mg;(3)2Fe;(4)N2;(5)2Na+;(6)$\stackrel{-2}{S{O}_{4}}$;(7)Al(OH)3;(8)Ca(NO3)2;(9)Al2(SO4)3;(10)FeCl2
(11)2H2;(12)K2CO3;(13)CuO;(14)4CO32-;(15)HNO3.
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础.

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案| A. | 向水中加明矾的作用是使悬浮物沉淀 | |
| B. | 常用的净水方法有吸附、沉淀、过滤、蒸发,其中蒸发的净化程度最高 | |
| C. | 用肥皂水可以区分硬水和软水,如果泡沫少是硬水,浮渣少则是软水 | |
| D. | 利用活性炭吸附水中的杂质,可以使水软化,是物理变化 |

| A. | 生成氧气的质量与加热氯酸钾和二氧化锰的混合物的时间关系 | |
| B. | 二氧化锰在固体混合物中质量变化情况 | |
| C. | 加热氯酸钾的对比情况:a添加了二氧化锰,b未添加二氧化锰 | |
| D. | 二氧化锰在固体混合物中质量分数的变化情况 |
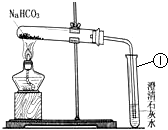 碳酸氢钠(NaHCO3)是一种重要的盐类物质,在生活中用途广泛.小洪同学设计实验对碳酸氢钠的性质进行了探究,请你参与她的探究活动.
碳酸氢钠(NaHCO3)是一种重要的盐类物质,在生活中用途广泛.小洪同学设计实验对碳酸氢钠的性质进行了探究,请你参与她的探究活动.【探究实验1】碳酸氢钠溶液的酸碱性.
【实验方案】取少量该固体加入试管中,加适量水溶解,再滴入几滴酚酞试液,振荡.
现象:溶液变成浅红色.
结论:碳酸氢钠溶液的碱性.
【探究实验2】碳酸氢钠的热稳定性.
【实验方案】设计实验装置如图,并进行实验.
现象:试管口有水珠,澄清石灰水变浑浊.充分加热后,试管中留下白色固体.
结论:碳酸氢钠受热有二氧化碳、水和白色固体生成.试管①中反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
小洪的同学认为:充分加热后的固体产物可能是NaOH或Na2CO3或NaOH和Na2CO3的混合物.
Ⅰ.他的依据是反应前后元素的种类不变.
Ⅱ.小洪同学为了确定反应后的固体产物成分进行以下实验,请填写下表:
| 实 验 | 实验现象 | 结 论 |
| 实验一:取少量反应后的固体产物溶于水,滴入几滴酚酞试液. | 溶液变成红色 | 固体产物一定是NaOH |
| 实验二:取少量反应后的固体产物溶于水,加入过量氯化钙溶液. | 产生了白色沉淀 | 固体产物含有Na2CO3. |
| 实验三:取实验二所得的上层清液于试管中,滴加酚酞试液. | 溶液不变色 | 固体产物是Na2CO3,而不是NaOH |
【拓展应用】根据以上探究,请说出碳酸氢钠在日常生活中的一种用途:治疗胃酸过多症.
 在进行水的净化实验时,小红将浑浊的河水样品倒入烧杯中,先加入明矾粉搅拌溶解,静置一段时间后,按图中装置进行过滤,请回答.
在进行水的净化实验时,小红将浑浊的河水样品倒入烧杯中,先加入明矾粉搅拌溶解,静置一段时间后,按图中装置进行过滤,请回答. 实验室常用制取氧气的方法有:a、加热氯酸钾;b、加热高锰酸钾固体;c、分解过氧化氢溶液,其实验装置如图所示.
实验室常用制取氧气的方法有:a、加热氯酸钾;b、加热高锰酸钾固体;c、分解过氧化氢溶液,其实验装置如图所示.