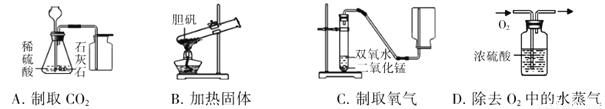
题目内容
甲、乙、丙三种固体物质的溶解度曲线如图所示.回答下列问题:
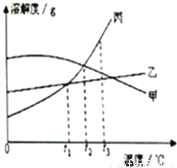
(1)t1℃时,三种物质的饱和溶液中溶质的质量分数由大到小的顺序是______;
(2)要将t2℃时甲的饱和溶液变成不饱和溶液,可采取的措施有:增加溶剂、______等.
(3)t3℃时,等质量的三种物质的饱和溶液降温到t1℃,析出晶体由大到小的顺序是______.
(4)乙中混有少量的丙,要提纯得到乙应采用___________________的结晶方法。
甲>乙=丙 降温 丙>乙>甲 蒸发溶剂 【解析】(1)t1℃时,因为在该温度下三种物质的溶解度由大到小顺序为甲>乙=丙,水都是100g,所以A、B、C三种固体物质的饱和溶液中,溶质的质量分数由大到小的顺序是甲>乙=丙; (2)由于甲物质的溶解度随温度的升高而减小,要将t2℃时甲的饱和溶液变成不饱和溶液,可采取降温的方法; (3)三种物质中只有甲物质的溶解度随温度的升高而减小,乙物... 阅读快车系列答案
阅读快车系列答案下列实验操作、现象与结论对应关系正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 向醋酸中加入氢氧化钠溶液 | 无明显现象 | 二者之间不发生反应 |
B | 向溶质质量分数为5%的过氧化氢溶液中加入少量氧化铜 | 有大量气泡产生 | 氧化铜起催化作用 |
C | 将两根铁丝分别伸入硫酸铜溶液和硝酸银溶液中 | 两根铁丝上均有固体附着 | 金属的活动性顺序为 Fe>Cu>Ag |
D | 用导管分别对准浸没在热水和冷水中的白磷通气 | 热水中的白磷燃烧,冷水中的白磷不燃烧 | .燃烧的条件之一是温度达到着火点 |
A. A B. B C. C D. D
D 【解析】A、向醋酸中加入氢氧化钠溶液,二者之间发生中和反应,但反应无明显现象,常需要借助于酸碱指示剂判断反应的发生,错误; B、催化剂的作用叫催化作用。催化剂就是能改变其它物质的反应速率,而本身的质量和化学性质在反应前后不变的物质。向溶质质量分数为5%的过氧化氢溶液中加入少量氧化铜,有大量气泡产生,但没有证明反应前后氧化铜的质量和化学性质不变,不能确定是催化剂,错误;C 、在金属活动性顺...为了探究石灰石的纯度(假设样品中的杂质既不溶于水也不与盐酸反应),称取80g石灰石样品等分为4份(分别编号为①、②、③、④),每份样品分别与一定量的稀盐酸反应,所得数据如表所示:
样品编号 | ① | ② | ③ | ④ |
稀盐酸的质量 | 50g | 100g | m(150<m<250) | 250g |
剩余固体的质量 | 15g | 10g | 4g | 4g |
然后,为了探究石灰石与稀盐酸反应后所得溶液中的溶质成分,将编号③所得溶液过滤,取滤液质量的1/8于烧杯中,向其中滴加质量分数为10.6%的碳酸钠溶液使其充分反应直至过量,有关的变化如图所示:
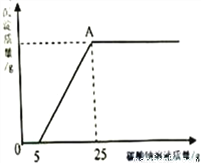
分析题中有关信息和图表(横坐标表示碳酸钠溶液、纵坐标为生成沉淀质量),回答下列问题:
(1)该石灰石样品的纯度为______.所用盐酸的溶质质量分数为__________。
(2)编号③所用稀盐酸的质量m为______g.
(3)A点处对应的溶液中溶质的质量是________?(写出计算过程)
80% 7.3% 200克 29.25克 【解析】【解析】 (1)该石灰石样品的纯度为×100%=80%; 50g盐酸消耗的碳酸钙质量为20g-15g=5g,设50g盐酸的溶质质量为x CaCO3+2HCl=CaCl2+H2O+CO2↑ 100 73 5g x x=3.65g 所用盐酸的溶质质量分数为×100%=7.3%; (2)设编号③...某兴趣小组在准备化学实验基本技能考试时,对以下问题进行了探究。
I.探究酸和碱能否发生化学反应
(1)方案l:甲同学向盛有少量NaOH溶液的试管中滴几滴无色酚酞试液,振荡,继续加入稀硫酸,观察到溶液由________色变成无色。甲同学得出结论:酸和碱能发生反应。
方案2:乙同学取少量NaOH溶液,测得溶液pH为10,向该溶液中加入一定量稀硫酸后,测得溶液pH为9,乙同学发现溶液pH减小了,得出结论:酸和碱能发生反应。
(2)交流讨论:大家同意甲同学的结论,对乙同学的实验过程提出质疑,溶液pH减小的原因还可能是稀硫酸中的水稀释了NaOH溶液;大家认为,乙同学向NaOH溶液中加入稀硫酸后,测得溶液的pH必须________7(填“大于”、“小于”或“等于”),才能证明酸和碱能发生反应。
II.探究酸和碱反应后溶液中溶质的成分
丙同学对探究I中甲同学实验后的无色溶液展开探究。
【提出问题】试管中无色溶液的溶质除了酚酞还有什么?
【提出猜想】猜想(l):Na2SO4;猜想(2):Na2SO4和____________。
【设计实验】现实验室提供以下试剂:锌粒、铜片、氯化钡溶液、氢氧化钠溶液以及必要的实验仪器,请完成下列表格:
实验操作 | 实验现象 | 实验结论 |
_____________ | _________ | 猜想(2)成立 |
【实验结论】猜想(2)成立
红 等于或小于 H2SO4 取适量甲同学实验反应后的溶液于试管中,加入锌粒,观察现象 锌粒溶解,并有气泡产生 【解析】本题考查了中和反应,酸、碱的化学性质。 Ⅰ、方案l:氢氧化钠溶液显碱性,滴入无色酚酞试液变红色,继续加入稀硫酸,硫酸与氢氧化钠发生中和反应生成硫酸钠和水,当加入的硫酸将氢氧化钠完全中和后,溶液变成无色,得出结论:酸和碱能发生反应; 方案2:溶液pH减小的原因还可能...