题目内容
4.酸、碱、盐是有广泛用途的重要化合物.某化学活动小组的同学围绕这几类化合物进行了一系列的探究活动.
(1)同学们打开盛浓盐酸和浓硫酸试剂瓶的瓶盖,立即就能把它们区分开来,这是为什么?
(2)如图是某试剂瓶标签上的内容.要把10 g这种浓硫酸稀释为20%的硫酸,需要水的质量为39g.稀释浓硫酸时,不可将水倒进浓硫酸里,请解释其原因.
(3)某化学学习小组的同学围绕:“澄清石灰水与碳酸钠溶液的反应”展开了如下探究活动.
①该反应的化学方程式为Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
②反应后溶液中的溶质是什么?同学们一致认为有以下三种情况:
A氢氧化钠和氢氧化钙; B氢氧化钠和碳酸钠;C氢氧化钠.
③小新取少量溶液于试管中,滴加过量稀盐酸,发现无气泡产生,说明情况②(填序号)是不可能的
为了进一步确定溶液的成分,同学们设计了如下实验方案:
| 实验步骤 | 现象 | 结论 |
| 取少量溶液于试管中,加入少量Na2CO3溶液 | 产生白色沉淀 | 情况①正确 |
(4)小政同学在整理实验台时,发现一瓶敞口放置的氢氧化钠固体,他猜想这瓶氢氧化钠可能变质,为了验证自己的猜想,和测出样品中氢氧化钠的质量分数,他做了如下实验:取该样品10克配成溶液,加入足量澄清石灰水,得到白色沉淀5克.请你帮助小政计算出该瓶样品中氢氧化钠的质量分数.
分析 (1)根据浓盐酸具有挥发性,浓硫酸具有吸水性,进行分析解答.
(2)根据溶液稀释前后,溶质的质量不变,结合题意进行分析解答.
(3)碳酸钠与氢氧化钙反应生成了碳酸钙沉淀和氢氧化钠,根据反应物的量分析反应后溶液中的溶质;根据碳酸钠与盐酸的反应、氢氧化钙与碳酸钠、二氧化碳的反应分析碳酸钠、氢氧化钙的存在情况;
(4)根据氢氧化钠与碳酸钠的性质,氢氧化钠与澄清石灰水不反应,碳酸钠与石灰水生成碳酸钙沉淀和氢氧化钠,根据反应的化学方程式,由生成碳酸钙沉淀的质量计算出样品中的碳酸钠,然后在求出样品中氢氧化钠的质量分数.
解答 解:(1)浓盐酸具有挥发性,打开盛浓盐酸的瓶盖有白雾出现;浓硫酸具有吸水性,打开瓶盖,无明显变化;可以鉴别.
(2)设要加水的质量为x,根据溶液稀释前后,溶质的质量不变,则
10g×98%=(10g+x)×20% 解得:x=39g.
稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;切不可把水注入浓硫酸中,这是因为浓硫酸的密度比水大,如果添加顺序颠倒,那么水会浮在水面上,又由于浓硫酸溶于水放出大量的热,能使水沸腾,容易造成酸液飞溅.
(3)①碳酸钠与氢氧化钙反应生成了碳酸钙沉淀和氢氧化钠,该反应的化学方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
②当碳酸钠与氢氧化钙签好反应时.反应后溶液中的溶质只有氢氧化钠,所以,同学们猜想C是溶液中只有氢氧化钠.
③由于碳酸钠能与盐酸反应生成了二氧化碳气体,所以小新取少量溶液于试管中,滴加过量稀盐酸,发现无气泡产生,说明情况②是不可能的
由于氢氧化钙能与碳酸钠反应生成碳酸钙沉淀,所以,为了进一步确定溶液的成分,同学们设计了如下实验方案:
| 实验步骤 | 现象 | 结论 |
| 取少量溶液于试管中,加入少量Na2CO3溶液 | 产生白色沉淀 | 情况①正确 |
(4)设样品中碳酸钠的质量为x
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
106 100
x 5.0g
$\frac{106}{100}=\frac{x}{5.0g}$ 解得:x=5.3g
样品中NaOH的质量分数=$\frac{10.0g-5.3g}{10.0g}$×l00%=47.0%
故答案为:(1)浓盐酸有挥发性,瓶口有白雾出现的是浓盐酸;(2)39;浓硫酸的密度比水大,水会浮在水面上,浓硫酸溶于水放出大量的热,能使水沸腾,容易造成酸液飞溅.(3)①Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.②氢氧化钠.③,②,见上表;(4)该瓶样品中氢氧化钠的质量分数位47.0%.
点评 本题难度不大,掌握酸的物理性质、溶液稀释前后溶质的质量不变、稀释浓硫酸的方法是正确解答本题的关键.

| A. | 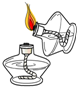 点燃酒精灯 | B. | 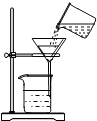 过滤 | ||
| C. | 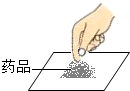 取粉末状固体药品 | D. | 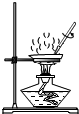 蒸发 |
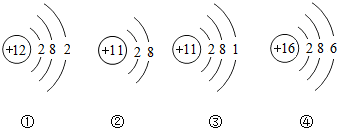
| A. | ①② | B. | ①③ | C. | ③④ | D. | ②④ |
【猜想与假设】根据沼气的成分猜想玉米秸秆中主要含有碳元素、氢元素.
【设计方案进行探究】
| 探究步骤 | 预计方案 | 相关结论 |
| 1、用坩埚钳夹持一小段烘干的玉米秸秆,点燃后伸入盛有氧气的集气瓶中 | 玉米秸秆剧烈燃烧,火焰熄灭后能够观察到瓶壁有水珠 | 产物中有水 |
| 2、向集气瓶中滴入少量澄清的石灰水 | 能够观察到石灰水变浑浊 | 产物中有CO2 |
(1)玉米秸秆烘干的目的是:①干燥,使其容易燃烧;②排出玉米秸秆中含有的水对实验的干扰
(2)根据以上探究,同学们得出结论:秸秆中含有C、H、O三种元素.
【反思与评价】你认为同学们得出的结论是否正确不正确,理由是氧元素可以来自于玉米秸秆,也可以来自于氧气,所以玉米秸秆中不一定含有氧元素.
【拓展与应用】
(1)该实验中用到的两个玻璃仪器是:集气瓶、胶头滴管.
(2)写出甲烷燃烧的方程式:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(3)农村的大部分地区处理玉米秸秆的方式是直接烧掉,试从环境、原料利用等方面说明玉米秸秆制沼气的重要意义(写一点即可)保护环境,变废为宝.
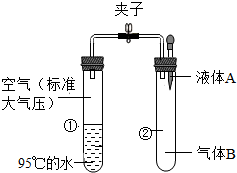 如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B的组合不可能的是下列的( )
如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B的组合不可能的是下列的( )| A. | 稀硫酸、氨气 | B. | 水、一氧化碳 | ||
| C. | 硝酸银溶液、氯化氢 | D. | 氢氧化钠溶液、二氧化碳 |
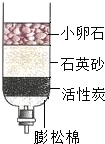 2010年,云南省遭遇了百年一遇的旱情,给工农业生产和生活用水带来了严重困难.为缓解旱情,有关部门实施了人工降雨.李斌同学利用所学知识将浑浊的水用右图所示的简易净水器进行净化,请根据你掌握的知识回答:
2010年,云南省遭遇了百年一遇的旱情,给工农业生产和生活用水带来了严重困难.为缓解旱情,有关部门实施了人工降雨.李斌同学利用所学知识将浑浊的水用右图所示的简易净水器进行净化,请根据你掌握的知识回答: