题目内容
8.电石的主要成分是碳化钙(CaC2),它与水反应生成氢氧化钙和乙炔(C2H2属于有机物).乙炔在氧气中完全燃烧的火焰(氧炔馅)温度很高,用于焊接和切割金属.写出制备乙炔、乙炔燃烧的化学方程式,并计算完全燃烧1300g乙炔要消耗多少克氧气.分析 根据题意,碳化钙与水反应生成氢氧化钙和乙炔,乙炔在氧气中完全燃烧生成二氧化碳和水,写出反应的化学方程式即可.
由参加反应的乙炔的质量,由反应的化学方程式列式计算出需要氧气的质量即可.
解答 解:碳化钙与水反应生成氢氧化钙和乙炔,反应的化学方程式为CaC2+2H2O═Ca(OH)2+C2H2↑.
乙炔在氧气中完全燃烧生成二氧化碳和水,反应的化学方程式为2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O.
设需要氧气的质量为x
2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O
52 160
1300g x
$\frac{52}{160}=\frac{1300g}{x}$ x=4000g
答:CaC2+2H2O═Ca(OH)2+C2H2↑;2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O;
完全燃烧1300g乙炔要消耗4000克氧气.
点评 本题难度不大,掌握利用化学方程式的计算方法、化学方程式的书写方法并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
19.要除去下列物质中混有的少量杂质(括号内为杂质),所用试剂和操作都正确的是( )
| A | CaCl2固体(CaCO3) | 加足量稀硫酸,蒸发、结晶 |
| B | NaCl固体(Na2CO3) | 加足量稀盐酸,蒸发、结晶 |
| C | Fe粉(Cu) | 加足量稀盐酸,过滤、洗涤、干燥 |
| D | NaCl固体(泥沙) | 加足量水溶解,过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
16.在Mg、MgO、Mg(OH)2、H2SO4和CuSO4溶液中,能生成MgSO4的方法有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
13.下列氮肥中不属于铵态氮肥的是( )
| A. | CO(NH2)2 | B. | NH4HSO4 | C. | NH4HCO3 | D. | NH4NO3 |
20.下列物质中,不可以作为化学肥料的是( )
| A. | 食盐 | B. | 碳酸钾 | C. | 尿素 | D. | 硝酸铵 |
18.硅酸钠(Na2SiO3)是一种重要的工业粘合剂,其中硅元素的化合价是( )
| A. | +2 | B. | +3 | C. | +4 | D. | +5 |
18.小华和他的小组同学就空气中氧气的含量进行如下实验,请你参与他们的探究活动.
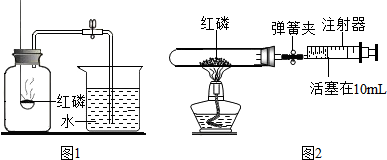
(1)当小华他们按如图1所示的装置和药品进行实验,如果实验成功,应观察到的现象是红磷燃烧,发出黄色火焰,冒大量白烟,同时放热
(2)实验后小华他们获得的数据见表.(注:本实验集气瓶的有效容积为1OOmL)根据数据通过计算得出氧气约占空气体积的17%,与21%有误差,造成这一结果的可能原因是①③.
①红磷的量不足,瓶内氧气没有消耗完
②没夹紧弹簧夹,红磷燃烧时瓶内空气膨胀导致部分空气从烧杯中的导管口逸出
③红磷燃烧结束并熄灭后,未等装置冷却就打开弹簧夹
④红磷在空气中引燃后,将燃烧匙插入瓶中并塞紧瓶塞时动作太慢,导致塞紧瓶塞之前瓶内部分空气受热逸出
(3)组内同学还对该实验进行了如下改进.(已知试管容积为45mL)
实验的操作步骤如下:
①点燃酒精灯;
②撤去酒精灯,待试管冷却后松开弹簧夹;
③将少量红磷平装入试管中,将20mL的注射器活塞置于1OmL刻度处,并按图2中所示的连接方式固定好,再将弹簧夹紧橡皮管;
④读取注射器活塞的数据.
正确的实验操作顺序是③①②④(填操作步骤的序号).如实验成功并含量测定准确,则注射器活塞将从lOmL刻度处慢慢前移到约为1mL刻度处才停止.

(1)当小华他们按如图1所示的装置和药品进行实验,如果实验成功,应观察到的现象是红磷燃烧,发出黄色火焰,冒大量白烟,同时放热
(2)实验后小华他们获得的数据见表.(注:本实验集气瓶的有效容积为1OOmL)根据数据通过计算得出氧气约占空气体积的17%,与21%有误差,造成这一结果的可能原因是①③.
①红磷的量不足,瓶内氧气没有消耗完
②没夹紧弹簧夹,红磷燃烧时瓶内空气膨胀导致部分空气从烧杯中的导管口逸出
③红磷燃烧结束并熄灭后,未等装置冷却就打开弹簧夹
④红磷在空气中引燃后,将燃烧匙插入瓶中并塞紧瓶塞时动作太慢,导致塞紧瓶塞之前瓶内部分空气受热逸出
| 组别 | 1 | 2 | 3 | 4 | 5 | 6 |
| 进入瓶中水的体积(mL) | 18 | 16 | 17 | 15 | 19 | 17 |
实验的操作步骤如下:
①点燃酒精灯;
②撤去酒精灯,待试管冷却后松开弹簧夹;
③将少量红磷平装入试管中,将20mL的注射器活塞置于1OmL刻度处,并按图2中所示的连接方式固定好,再将弹簧夹紧橡皮管;
④读取注射器活塞的数据.
正确的实验操作顺序是③①②④(填操作步骤的序号).如实验成功并含量测定准确,则注射器活塞将从lOmL刻度处慢慢前移到约为1mL刻度处才停止.