题目内容
19. 某环保小组监测到一湿法冶铜厂排放的废水中含有硫酸和硫酸铜两种污染物,为测定该废水中各污染物的含量,给冶铜厂提供处理废水的参考,环保小组的同学进行了以下实验:取废水500g,向其中加入溶质质量分数为20%的氢氧化钠溶液,测得沉淀质量与所加入的氢氧化钠溶液的质量关系如图,根据图中所得数据计算分析:
某环保小组监测到一湿法冶铜厂排放的废水中含有硫酸和硫酸铜两种污染物,为测定该废水中各污染物的含量,给冶铜厂提供处理废水的参考,环保小组的同学进行了以下实验:取废水500g,向其中加入溶质质量分数为20%的氢氧化钠溶液,测得沉淀质量与所加入的氢氧化钠溶液的质量关系如图,根据图中所得数据计算分析:(1)完全反应后的所得沉淀的化学式为Cu(OH)2;其质量为19.6g;
(2)计算该废水中硫酸铜的溶质质量分数.(请写出计算过程)
(3)氢氧化钠溶液滴至mg之前没有产生沉淀的原因是在与硫酸铜反应之前氢氧化钠优先与硫酸反应.
分析 (1)根据如图信息可知,反应生成的沉淀是氢氧化铜以及质量;
(2)根据氢氧化钠与硫酸铜反应的化学方程式,利用生成沉淀的物质的量可计算出废水中硫酸铜的物质的量,换算硫酸铜质量;
(3)根据氢氧化钠优先与硫酸反应解答.
解答 (1)根据如图可知,反应生成的沉淀是氢氧化铜,化学式为:Cu(OH)2;质量为19.6g;故填:Cu(OH)2;19.6;
(2)设废水中硫酸铜的物质的量为x,
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
160 98
x 19.6g
$\frac{160}{x}=\frac{98}{19.6g}$
x=32g;
该废水中硫酸铜的溶质质量分数为$\frac{32g}{500g}$×100%=6.4%
答:该废水中硫酸铜的溶质质量分数为6.4%.
(3)在与硫酸铜反应之前氢氧化钠优先与硫酸反应,所以氢氧化钠溶液滴至40g之前没有产生沉淀.
故填:在与硫酸铜反应之前氢氧化钠优先与硫酸反应.
点评 对反应的图象中曲线进行分析,该曲线的起点表示硫酸被完全反应、折点表示硫酸铜与氢氧化钠恰好完全反应.

练习册系列答案
相关题目
14.浓硫酸和浓盐酸敞口放置在空气中一段时间后,溶液中( )
| A. | 溶液的质量都增大 | |
| B. | 溶质的质量分数都变小 | |
| C. | 溶质的质量分数前者变大,后者变小 | |
| D. | 溶质的质量分数都变大 |
4.汽车尾气净化装置中装有铂催化剂,尾气在催化剂表面反应的微观过程可用如图表示.下列有关说法正确的是( )
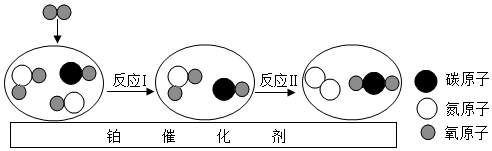

| A. | 反应I中的反应物分子有三种 | |
| B. | 反应Il属于置换反应 | |
| C. | 反应Il中参加反应的二氧化氮与一氧化碳的分子个数比为2:l | |
| D. | 此净化装置可以消除一氧化碳、一氧化氮、二氧化氮对空气的污染 |
11.如图是在密闭容器内发生化学前后微观粒子的变化情况,该化学反应的类型属( )

| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
8.化学在生产、生活中应用广泛,下列过程属于化学变化的是( )
| A. |  海水晒盐 | B. |  活性炭净水 | ||
| C. |  煤制煤气 | D. |  干冰降雨 |
9.通常情况下,铜不和稀硫酸反应,但是把一小块铜片放入适量稀硫酸中,同时加入X再加热,可以发生如下反应:2Cu+2H2SO4(稀)+X$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O,下列说法正确的是( )
| A. | 反应前后各元素的化合价没有变化 | B. | 反应物X的化学式是O2 | ||
| C. | 反应后溶液的质量减少 | D. | 反应后溶液会由蓝色变为无色 |

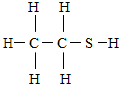 乙硫醇是 2016 年版吉尼斯世界纪录中收录的最臭的物质. 空气中仅含五百亿分之一的乙硫醇时,其臭味就可嗅到,通常被加入液化煤气中做臭味指示剂. 乙硫醇的结构式见图,请回答下列问题:
乙硫醇是 2016 年版吉尼斯世界纪录中收录的最臭的物质. 空气中仅含五百亿分之一的乙硫醇时,其臭味就可嗅到,通常被加入液化煤气中做臭味指示剂. 乙硫醇的结构式见图,请回答下列问题: