题目内容
5.生活离不开水.(1)茶杯内的网罩,可将茶水与茶叶分离,便于饮用,与该设计原理相似的化学实验操作是过滤;自制净水器中常加入活性炭用于除去水中的异味和色素;鉴别硬水和软水可选用肥皂水(填“石灰水”或“肥皂水”).
(2)ClO2是新一代饮用水的消毒剂C1O2应读作二氧化氯,C1O2中氯元素的化合价为+4,C1O2所属物质的类别是氧化物.
(3)在氯化钠的饱和溶液中,水是溶剂(填“溶质”或“溶剂”),要将氯化钠的饱和溶液变为不饱和溶液,可采用的方法是加水、升高温度(任填两种).
分析 (1)根据过滤的原理、活性炭的吸附性和硬水与软水的鉴别方法分析回答.
(2)根据ClO2的读法、组成和化合价原则分析回答;
(3)根据溶液的组成和饱和溶液与不饱和溶液的转化方法分析回答.
解答 解:(1)茶杯内的纱网能滤去茶叶,和过滤器除去水中泥沙原理是一样的;活性炭由吸附性,可用于除去水中的异味和色素;鉴别硬水和软水可选用肥皂水,遇肥皂水产生的泡沫少的是硬水,遇肥皂水产生的泡沫多的是软水.
(2)ClO2是新一代饮用水的消毒剂,C1O2应读作二氧化氯,C1O2中由于氧显-2价,氯元素的化合价为:+4 价,C1O2所属物质的类别是氧化物.
(3)在氯化钠的饱和溶液中,水是溶剂,要将氯化钠的饱和溶液变为不饱和溶液,可采用的方法是加水、升高温度等.
故答为:(1)过滤,活性炭,肥皂水;(2)二氧化氯,+4,氧化物;(3)溶剂,加水、升高温度等.
点评 本题较为简单,只考查了的知识属于课本中的基础知识,难度不大根据已有的知识分析解答即可.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
20. 2013年央视315晚会曝光周大生等品牌黄金掺假:所谓的千足金,很多都没达标,而是添加了另一种元素,叫做“铱”.铱在化学元素周期表中与黄金相邻,它的密度与黄金非常相似,但它的价格远比黄金便宜.从如图中不能得到的信息有( )
2013年央视315晚会曝光周大生等品牌黄金掺假:所谓的千足金,很多都没达标,而是添加了另一种元素,叫做“铱”.铱在化学元素周期表中与黄金相邻,它的密度与黄金非常相似,但它的价格远比黄金便宜.从如图中不能得到的信息有( )
 2013年央视315晚会曝光周大生等品牌黄金掺假:所谓的千足金,很多都没达标,而是添加了另一种元素,叫做“铱”.铱在化学元素周期表中与黄金相邻,它的密度与黄金非常相似,但它的价格远比黄金便宜.从如图中不能得到的信息有( )
2013年央视315晚会曝光周大生等品牌黄金掺假:所谓的千足金,很多都没达标,而是添加了另一种元素,叫做“铱”.铱在化学元素周期表中与黄金相邻,它的密度与黄金非常相似,但它的价格远比黄金便宜.从如图中不能得到的信息有( )| A. | 铱原子的质子数为77 | B. | 铱原子的中子数为77 | ||
| C. | 铱原子的核电荷数为77 | D. | 铱元素的元素符号为Ir |
10. 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?
在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
(1)实验准备
①查阅资料:NaHCO3+NaOH═Na2CO3+H2O
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
CaCl2+2NaOH═Ca(OH)2↓(微溶)+2NaCl
2NaHCO3(溶液)$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
NaHCO3+HCl═NaCl+H2O+CO2↑
Ca(OH)2+NaHCO3═CaCO3↓+NaOH+H2O
②前期实验:
用一定溶质的质量分数的NaHCO3、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考.
Ⅰ对应反应的化学方程式为HCl+NaOH═NaCl+H2O,
Ⅱ的现象为有沉淀产生.
(2)实验过程
【实验1】证明NaOH溶液与NaHCO3溶液反应生成了Na2CO3
同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是CaCl2.有同学提出这个实验不足以证明有Na2CO3生成,其理由是CaCl2 和NaOH反应生成Ca(OH)2,氢氧化钙是微溶物,在溶液中也产生沉淀.为了证明有Na2CO3生成,需要继续进行的操作是:取少量反应后的滤渣加入足量的取少量反应后滤渣加入足量的稀盐酸,若产生无色气体证明有Na2CO3生成,反之则没有,若产生无色气体证明有Na2CO3生成,反之则没有.
【实验2】证明NaOH溶液与NaHCO3溶液反应后NaHCO3不存在
同学们参考上表中的实验,又设计了一个实验,虽然没有观察到明显的实验现象,但可以证明反应发生了,该实验方案是取少量反应后的溶液进行取少量反应后的溶液加热至沸腾(填操作),将产生的气体通入澄清石灰水,若澄清石灰水变浑浊,证明有NaHCO3存在,反之则没有.
(3)实验反思
通过实验1和实验2说明,对于没有明显现象的化学反应,可以从不同的角度证明反应的发生,比如:一是可以通过反应物检验证明反应发生;二是可以通过产物检验证明反应发生.
 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
(1)实验准备
①查阅资料:NaHCO3+NaOH═Na2CO3+H2O
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
CaCl2+2NaOH═Ca(OH)2↓(微溶)+2NaCl
2NaHCO3(溶液)$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
NaHCO3+HCl═NaCl+H2O+CO2↑
Ca(OH)2+NaHCO3═CaCO3↓+NaOH+H2O
②前期实验:
用一定溶质的质量分数的NaHCO3、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考.
| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | 产生气泡 | Ⅰ | 产生气泡 |
| 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | Ⅱ |
| 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
Ⅱ的现象为有沉淀产生.
(2)实验过程
【实验1】证明NaOH溶液与NaHCO3溶液反应生成了Na2CO3
同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是CaCl2.有同学提出这个实验不足以证明有Na2CO3生成,其理由是CaCl2 和NaOH反应生成Ca(OH)2,氢氧化钙是微溶物,在溶液中也产生沉淀.为了证明有Na2CO3生成,需要继续进行的操作是:取少量反应后的滤渣加入足量的取少量反应后滤渣加入足量的稀盐酸,若产生无色气体证明有Na2CO3生成,反之则没有,若产生无色气体证明有Na2CO3生成,反之则没有.
【实验2】证明NaOH溶液与NaHCO3溶液反应后NaHCO3不存在
同学们参考上表中的实验,又设计了一个实验,虽然没有观察到明显的实验现象,但可以证明反应发生了,该实验方案是取少量反应后的溶液进行取少量反应后的溶液加热至沸腾(填操作),将产生的气体通入澄清石灰水,若澄清石灰水变浑浊,证明有NaHCO3存在,反之则没有.
(3)实验反思
通过实验1和实验2说明,对于没有明显现象的化学反应,可以从不同的角度证明反应的发生,比如:一是可以通过反应物检验证明反应发生;二是可以通过产物检验证明反应发生.
17.葡萄糖能给我们带来甜蜜和健康,化学式C6H12O6下列有关说法错误的是( )
| A. | 糖类俗称“碳水化合物”,说明葡萄糖就是由C和H2O组成的混合物 | |
| B. | 葡萄糖由碳、氢、氧三种元素组成 | |
| C. | 葡萄糖中碳、氢、氧三种元素的质量比为6:1:8 | |
| D. | 除葡萄糖所属的糖类外,六大营养素还包括蛋白质、油脂、维生素、无机盐和水 |
6.下列实验现象的描述正确的是( )
| A. | 蜡烛在空气中燃烧生成二氧化碳和水 | |
| B. | 硫在空气中燃烧,发出明亮的蓝紫色火焰 | |
| C. | 木炭在氧气中燃烧,发出黄色火焰,生成有刺激性气味的气体 | |
| D. | 氢气在空气中燃烧发出淡蓝色火焰 |
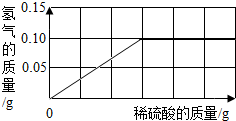 为测定黄铜(铜锌合金)的组成,现取10g黄铜样品与足量的稀硫酸反应至刚好不在产生气体为止,反应过程中产生气体的质量与所用稀硫酸的质量关系如图所示:计算:
为测定黄铜(铜锌合金)的组成,现取10g黄铜样品与足量的稀硫酸反应至刚好不在产生气体为止,反应过程中产生气体的质量与所用稀硫酸的质量关系如图所示:计算: