题目内容
(2012?南平)实验室配制16%的氯化钠溶液100g.
(1)在①溶解、②称量和③计算这三步操作中,正确的顺序是
(2)配制时要称取氯化钠
(3)量取蒸馏水时使用的量筒规格是
(1)在①溶解、②称量和③计算这三步操作中,正确的顺序是
③②①
③②①
(填序号).(2)配制时要称取氯化钠
16
16
g.(3)量取蒸馏水时使用的量筒规格是
100mL
100mL
(选填“100mL”或“50mL”或“10mL”).分析:(1)根据配制溶质质量分数一定的溶液的基本步骤进行分析解答.
(2)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量.
(3)再根据溶剂质量=溶液质量-溶质质量即可求得蒸馏水的质量,进而计算出水的体积,确定量取蒸馏水时使用的量筒规格.
(2)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量.
(3)再根据溶剂质量=溶液质量-溶质质量即可求得蒸馏水的质量,进而计算出水的体积,确定量取蒸馏水时使用的量筒规格.
解答:解:(1)配制一定质量分数的溶液的步骤:计算、称量(量取)、溶解.
(2)溶质质量=溶液质量×溶质的质量分数,配制16%的氯化钠溶液100g,需氯化钠的质量=100g×16%=16g.
(3)溶剂质量=溶液质量-溶质质量,则所需蒸馏水的质量=100g-16g=84g;水的密度为水的密度为1g/cm3,则根据V=
=
=84cm3=84mL,故量取蒸馏水时应使用100mL的量筒.
故答案为:(1)③②①;(2)16;(3)100mL.
(2)溶质质量=溶液质量×溶质的质量分数,配制16%的氯化钠溶液100g,需氯化钠的质量=100g×16%=16g.
(3)溶剂质量=溶液质量-溶质质量,则所需蒸馏水的质量=100g-16g=84g;水的密度为水的密度为1g/cm3,则根据V=
| m |
| ρ |
| 84g |
| 1g/cm3 |
故答案为:(1)③②①;(2)16;(3)100mL.
点评:本题难度不是很大,掌握配制溶质质量分数一定的溶液的基本步骤、量筒的使用等是正确解答本题的关键.

练习册系列答案
相关题目
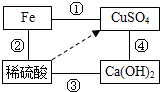 (2012?南平)如图实线“--”表示相连的两种物质间会发生化学反应,据图回答:
(2012?南平)如图实线“--”表示相连的两种物质间会发生化学反应,据图回答: