题目内容
6.下列实验现象描述错误的是( )| A. | 铁丝在氧气中燃烧火星四射 | |
| B. | 二氧化碳通入紫色石蕊试液,试液变红 | |
| C. | 铁丝浸入硫酸铜溶液中表面有红色物质生成 | |
| D. | 红磷在氧气中燃烧产生白雾 |
分析 A、根据铁丝在氧气中燃烧的现象进行分析判断.
B、根据二氧化碳的化学性质进行分析判断.
C、根据铁丝在氧气中燃烧的现象进行分析判断.
D、根据红磷在氧气中燃烧的现象进行分析判断.
解答 解:A、铁丝在氧气中剧烈燃烧,火星四射,故选项说法正确.
B、二氧化碳与水反应生成碳酸,碳酸能使紫色石蕊试液变红色,二氧化碳通入紫色石蕊试液,试液变红,故选项说法正确.
C、铁的金属活动性比铜强,能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,铁丝浸入硫酸铜溶液中表面有红色物质生成,故选项说法正确.
D、红磷在氧气中燃烧,产生大量的白烟,而不是白雾,故选项说法错误.
故选:D.
点评 本题难度不大,掌握常见物质燃烧的现象、二氧化碳的化学性质、金属的化学性质即可正确解答,在描述实验现象时,需要注意烟和雾的区别.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.下列微粒结构示意图中,能表示阴离子的是( )
| A. |  | B. |  | C. |  | D. | 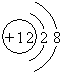 |
11.以下摘录的是某些同学对所学知识的整理归纳,你认为正确的是( )
| A. | 合金含两种或两种以上金属 | |
| B. | 含有氧元素的化合物都属于氧化物 | |
| C. | 酸碱中和生成盐和水,所以盐溶液都为中性 | |
| D. | 若使可燃物的温度降到着火点以下就能灭火 |
18.下列有关各种气体的描述以及对应的用途,其因果关系及描述完全正确的是( )
| A. | 氧气是一种极易溶于水的气体,鱼类可以在水中生存 | |
| B. | 氮气由氮元素组成,可用于医疗麻醉 | |
| C. | 稀有气体化学性质不活泼,用作保护气 | |
| D. | 二氧化碳不支持燃烧,可用于制造汽水 |
15.下列哪种金属可以和其它三种金属的盐溶液反应的是( )
| A. | Mg | B. | Ag | C. | Cu | D. | Zn |