题目内容
14.用适当的数字和符号和化学式填空:(1)三个钾原子3K;(2)一个碳酸根离子CO32-.
(3)固体“干冰”CO2;(4)酒精C2H5OH;(5)可用于炼铁的有毒气体是CO.
分析 (1)原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.
(2)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字.
(3)固体“干冰”是固态的二氧化碳,写出其化学式即可.
(4)由常见有机物的化学式进行书写即可.
(5)一氧化碳具有还原性,是可用于炼铁的有毒气体.
解答 解:(1)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故三个钾原子表示为:3K.
(2)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字,故一个碳酸根离子可表示为:CO32-.
(3)固体“干冰”是固态的二氧化碳,其化学式为:CO2.
(4)酒精的化学式为:C2H5OH.
(5)一氧化碳具有还原性,是可用于炼铁的有毒气体,其化学式为:CO.
故答案为:(1)3K;(2)CO32-;(3)CO2;(4)C2H5OH;(5)CO.
点评 本题难度不大,掌握常见化学用语(原子符号、分子符号、化学式等)的书写方法是正确解答此类题的关键.

练习册系列答案
相关题目
5.量筒内液体读数,开始时仰视读数为29.0ml,倒出一部分液体后,平视读数为11.6ml,则实际倒出液体的体积为( )
| A. | 大于17.4ml | B. | 等于17.4ml | C. | 少于17.4ml | D. | 无法计算 |
2.下列有关实验现象和数据处理的描述,正确的是( )
| A. | 镁条在空气中燃烧,发出耀眼的白光,生成白色固体 | |
| B. | 用托盘天平称取22.26g食盐 | |
| C. | 木炭在氧气中燃烧,生成有刺激性气味的气体 | |
| D. | 蜡烛在氧气中燃烧发出白光,放出热量,生成二氧化碳和水 |
19. 钢铁工业是国家工业的基础.
钢铁工业是国家工业的基础.
I.如图是教材中炼铁高炉及炉内化学变化过程示意图,根据图示回答下列问题.
若如图中采用的铁矿石的主要成分为氧化铁,请写出A区所发生主要反应的化学方程式:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
II.化学兴趣小组同学在实验室里利用碳和氧化铁反应模拟炼铁,得到了无色气体A和黑色粉末B,并探究两者的成分.

(一)甲组同学对无色气体A的成分进行探究.
【猜想与假设】
猜想1:A中只有CO2; 猜想2:A中只有CO; 猜想3:A中有CO2和CO.
【实验验证】
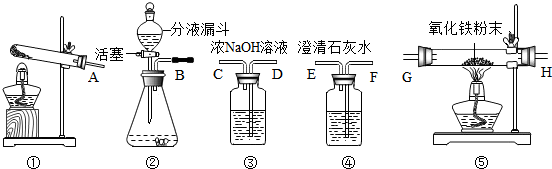
甲组同学按如图示进行实验(箭头表示气体流向,NaOH溶液的作用是除去气体中的CO2).

【讨论交流】
实验证实猜想3正确,则:
(1)Ⅰ中澄清石灰水的作用是检验CO2,能证明猜想3成立的现象是Ⅰ中澄清石灰水变浑浊,Ⅲ中黑色固体变为红色(或I、Ⅳ中澄清石灰水均变浑浊).
(2)Ⅲ中反应的化学方程式CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
(二)乙组同学对黑色粉末B的成分进行探究.
【查阅资料】
①碳(或一氧化碳)还原氧化铁的固体产物可能有四氧化三铁、氧化亚铁、铁.
②碳(或一氧化碳)还原氧化铁的产物成分与反应温度、反应时间等因素有关.
③
【初步实验与猜想】
①小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和氧化亚铁(或FeO).
②进行猜想:黑色固体粉末可能是:
猜想一:全部是Fe;猜想二:全部是Fe3O4;猜想三:是Fe和Fe3O4的混合物.
【进一步实验】该小组按右图装置设计实验,在一定温度下进行了实验,测得下列数据:

①应前称取5.8g黑色粉末B加入玻璃管内 (玻璃管的质量为60.0g)
②充分反应后管内固体全部是铁,玻璃管和管内固体的总质量64.2g(已冷却到室温).
【得出结论】根据上述数据,经计算得出该黑色粉末B是Fe3O4.
【反思与评价】碳(或一氧化碳)还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间.
 钢铁工业是国家工业的基础.
钢铁工业是国家工业的基础.I.如图是教材中炼铁高炉及炉内化学变化过程示意图,根据图示回答下列问题.
若如图中采用的铁矿石的主要成分为氧化铁,请写出A区所发生主要反应的化学方程式:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
II.化学兴趣小组同学在实验室里利用碳和氧化铁反应模拟炼铁,得到了无色气体A和黑色粉末B,并探究两者的成分.

(一)甲组同学对无色气体A的成分进行探究.
【猜想与假设】
猜想1:A中只有CO2; 猜想2:A中只有CO; 猜想3:A中有CO2和CO.
【实验验证】
甲组同学按如图示进行实验(箭头表示气体流向,NaOH溶液的作用是除去气体中的CO2).

【讨论交流】
实验证实猜想3正确,则:
(1)Ⅰ中澄清石灰水的作用是检验CO2,能证明猜想3成立的现象是Ⅰ中澄清石灰水变浑浊,Ⅲ中黑色固体变为红色(或I、Ⅳ中澄清石灰水均变浑浊).
(2)Ⅲ中反应的化学方程式CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
(二)乙组同学对黑色粉末B的成分进行探究.
【查阅资料】
①碳(或一氧化碳)还原氧化铁的固体产物可能有四氧化三铁、氧化亚铁、铁.
②碳(或一氧化碳)还原氧化铁的产物成分与反应温度、反应时间等因素有关.
③
| 物质 性质 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
①小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和氧化亚铁(或FeO).
②进行猜想:黑色固体粉末可能是:
猜想一:全部是Fe;猜想二:全部是Fe3O4;猜想三:是Fe和Fe3O4的混合物.
【进一步实验】该小组按右图装置设计实验,在一定温度下进行了实验,测得下列数据:

①应前称取5.8g黑色粉末B加入玻璃管内 (玻璃管的质量为60.0g)
②充分反应后管内固体全部是铁,玻璃管和管内固体的总质量64.2g(已冷却到室温).
【得出结论】根据上述数据,经计算得出该黑色粉末B是Fe3O4.
【反思与评价】碳(或一氧化碳)还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间.
3.现有下列仪器;①.10ml量筒 ②.50ml量筒 ③.试管 ④.胶头滴管 ⑤.天平,欲取40ml的液体,应选用的仪器是( )
| A. | ①④ | B. | ②⑤ | C. | ②④ | D. | ③④ |
4.“珍爱生命,远离毒品”.冰毒是一种毒品,其主要成分是甲基苯丙胺(化学式为C10H15N).有关甲基苯丙胺的说法正确的是( )
| A. | 甲基苯丙胺的相对分子质量为150 | |
| B. | 甲基苯丙胺属于化合物 | |
| C. | 一个甲基苯丙胺分子中有25个原子 | |
| D. | 甲基苯丙胺中氢元素的质量分数最大 |