题目内容
发射通讯卫星的火箭用联氨(N2H4)做燃料,用四氧二氮(N2O4)助燃,生成物不会对大气造成污染.反应的化学方程式为:2N2H4+N2O4═3 +4H2O,请在横线上填写化学式以完成该化学方程式.
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:根据质量守恒定律,化学变化前后原子的种类不变、原子个数没有增减,结合化学方程式2N2H4+N2O4═3X+4H2O从而推断X的化学式.
解答:解:根据质量守恒定律,化学变化前后原子的种类不变、原子个数没有增减.从化学方程式2N2H4+N2O4═3X+4H2O看,反应前反应物中N、H、O元素的原子个数依次为:6、8、4;反应后生成物中除3X外,H、O元素的原子个数为8、4.比较反应前后原子种类及个数可得知,3X中应含有6个N原子,所以X的化学式为N2.
故答案为:
2N2H4+N2O4═3N2+4H2O.
故答案为:
2N2H4+N2O4═3N2+4H2O.
点评:本题是运用化学中的基本思想质量守恒思想,利用化学方程式进行计算,从而推断出物质的化学式.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
在CuCl2和MgCl2混合溶液中加入过量的铁粉,充分反应后过滤,滤纸上留下的物质是( )
| A、Fe | B、Mg |
| C、Cu | D、无法确定 |
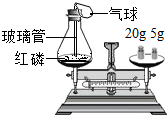 为了研究质量守恒定律,设计了图“红磷燃烧前后质量测定”的实验,请分析有关问题:
为了研究质量守恒定律,设计了图“红磷燃烧前后质量测定”的实验,请分析有关问题: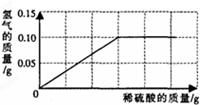 为了测定黄铜(铜、锌合金)组成,某研究性学习小组称取该样品10g,向其中逐滴加入稀硫酸至刚好不再产生气体为止.反应过程中生成的气体与所用硫酸溶液的质量关系如图所示.试计算样品中铜的质量分数.
为了测定黄铜(铜、锌合金)组成,某研究性学习小组称取该样品10g,向其中逐滴加入稀硫酸至刚好不再产生气体为止.反应过程中生成的气体与所用硫酸溶液的质量关系如图所示.试计算样品中铜的质量分数.