题目内容
 某校研究性学习小组进行了一个有趣的实验探究:
某校研究性学习小组进行了一个有趣的实验探究:
提出问题:实验室有一瓶久置的NaOH,变质程度怎样?
设计方案:先称取21.2g 的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加
入一定质量分数的稀硫酸直至过量(Na2CO3+H2SO4═Na2SO4+H2O+CO2↑),根据生成CO2的质量计算出Na2CO3的质量,从而进一步确定样品中NaOH的质量分数.
进行实验:实验测得加入稀硫酸的质量与产生CO2气体的质量关系如图所示.
数据处理:写出以下计算过程:
(1)该样品中Na2CO3的质量为多少?
(2)该样品中NaOH的质量分数为多少?
反思与交流:从图中0~A点说明:在NaOH与Na2CO3的混合溶液中,加入强酸,首先反应的物质是______.
解:由图象可知,在检验样品中的杂质时加入稀硫酸,并无二氧化碳气体产生,原因是在碱性溶液中,硫酸与碱发生中和反应,不产生气体,当加入的硫酸的质量为50多克时,开始与样品中的碳酸钠发生反应,生成二氧化碳气体,并随着反应的进行,当继续滴加硫酸时,产生的气体为2.2g,并且不再变化,说明样品中的碳酸钠完全反应完毕,由此可根据二氧化碳的质量计算出样品的碳酸钠的质量,同些也可计算出原样品中氢氧化钠的质量,从而得出样品中氢氧化钠的质量分数.过程如下:
[数据处理]从图中得知:产生CO2的最大量为2.2g.
(1)解:设该样品中Na2CO3的质量为x,则:
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
106 44
x 2.2g
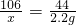
x=5.3g
(2)则样品中NaOH质量分数为: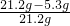 ×100%=75.0%;
×100%=75.0%;
[反思与交流]由图象可知开始加入硫酸时无气体生成,则一定是硫酸先于氢氧化钠反应,当硫酸反应完后在与碳酸钠反应生成二氧化碳;
故答案为:(1)答:样品中Na2CO3的质量为5.3g;(2)NaOH的质量分数为75.0%;NaOH;
分析:本题结合图象进行有关问题的探究,题目选择易与二氧化碳反应的碱性物质氢氧化钠的变质程度,并能计算样品的物质质量分数,解决此类问题关键是看明白图象的含义,注意图象中特殊的点的意义,然后结合题目条件,解答此类问题.
点评:本题综合考查了学生对图象问题的识别能力,近几年中考题中对此类问题的考查越来越多,解题关键还是要看明确图象所表示的意义,综合性较强,易出错.
[数据处理]从图中得知:产生CO2的最大量为2.2g.
(1)解:设该样品中Na2CO3的质量为x,则:
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
106 44
x 2.2g
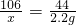
x=5.3g
(2)则样品中NaOH质量分数为:
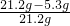 ×100%=75.0%;
×100%=75.0%;[反思与交流]由图象可知开始加入硫酸时无气体生成,则一定是硫酸先于氢氧化钠反应,当硫酸反应完后在与碳酸钠反应生成二氧化碳;
故答案为:(1)答:样品中Na2CO3的质量为5.3g;(2)NaOH的质量分数为75.0%;NaOH;
分析:本题结合图象进行有关问题的探究,题目选择易与二氧化碳反应的碱性物质氢氧化钠的变质程度,并能计算样品的物质质量分数,解决此类问题关键是看明白图象的含义,注意图象中特殊的点的意义,然后结合题目条件,解答此类问题.
点评:本题综合考查了学生对图象问题的识别能力,近几年中考题中对此类问题的考查越来越多,解题关键还是要看明确图象所表示的意义,综合性较强,易出错.

练习册系列答案
相关题目
某校研究性学习小组的同学设计了简单的实验方案,验证呼出的气体与吸入的气体成分的含量有什么不同,请将实验现象填入下表中的空格处:
| 实验步骤 | 实验现象 |
| 1、 用排水法收集两瓶呼出的气体, 另收集两瓶空气. | 不填 |
| 2、将澄清石灰水分别滴入盛有呼出的 气体和空气的集气瓶中,振荡. | 呼出的气体中石灰水_________ |
| 3、把燃着的木条放进余下两瓶气体中 | 先熄灭的是__________________ |
| 4、对头玻璃片吹气 | 玻璃上出现______________ |
最终得出的实验结论是__________________________________.
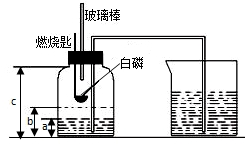 某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下:
某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下: 某校研究性学习小组到实验室进行探究实验.他们准备用加热高锰酸钾的方法制取氧气并验证氧气的性质.
某校研究性学习小组到实验室进行探究实验.他们准备用加热高锰酸钾的方法制取氧气并验证氧气的性质.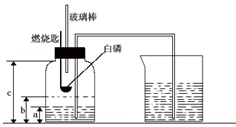 某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下:
某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下: