题目内容
2.向50g溶质的质量分数为10%的氢氧化钠溶液里加入10g的氢氧化钠或蒸发掉10g水,所得溶液的溶质质量分数为25%或12.5%.分析 根据溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%,进行分析解答.
解答 解:由溶质质量分数的计算公式:溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%可知:
向50g溶质的质量分数为10%的氢氧化钠溶液里加入10g的氢氧化钠,所得溶液的溶质质量分数为:$\frac{50g×10%+10g}{50g+10g}×100%$=25%
将50g溶质的质量分数为10%的氢氧化钠溶蒸发掉10g水,所得溶液的溶质质量分数为:$\frac{50g×10%}{50g-10g}×100%$=12.5%
故答为:25%,12.5%.
点评 本题主要考查了溶质质量分数的计算,在计算时容易出错的地方是没有分清溶液中的各个量的变化.

练习册系列答案
相关题目
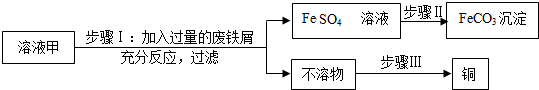
12.验证金属Fe、Cu和Ag的活动性强弱,下列方案不能达到目的是( )
| A. | FeSO4溶液 Cu Ag | B. | Fe CuSO4溶液 Ag | ||
| C. | Fe Cu AgNO3溶液 稀盐酸 | D. | FeSO4溶液 Cu AgNO3溶液 |
13.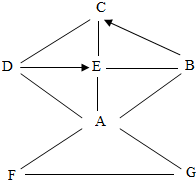 已知A、B、C、D、E、F、G均为初中化学常见的物质,相互关系如图所示,“→”表示转化关系,“一”表示相互之间能反应(部分反应物、生成物以及反应条件省略).其中,A是人体胃酸的主要成分;B为一种盐;C是一种常用来灭火的气体,过多排放会导致温室效应;D是一种常用的食品干燥剂也可用做建筑材料;组成G单质的元素在地壳中含量居所有金属元素的第二位.分析以上信息及图所示,以下分析错误的是( )
已知A、B、C、D、E、F、G均为初中化学常见的物质,相互关系如图所示,“→”表示转化关系,“一”表示相互之间能反应(部分反应物、生成物以及反应条件省略).其中,A是人体胃酸的主要成分;B为一种盐;C是一种常用来灭火的气体,过多排放会导致温室效应;D是一种常用的食品干燥剂也可用做建筑材料;组成G单质的元素在地壳中含量居所有金属元素的第二位.分析以上信息及图所示,以下分析错误的是( )
 已知A、B、C、D、E、F、G均为初中化学常见的物质,相互关系如图所示,“→”表示转化关系,“一”表示相互之间能反应(部分反应物、生成物以及反应条件省略).其中,A是人体胃酸的主要成分;B为一种盐;C是一种常用来灭火的气体,过多排放会导致温室效应;D是一种常用的食品干燥剂也可用做建筑材料;组成G单质的元素在地壳中含量居所有金属元素的第二位.分析以上信息及图所示,以下分析错误的是( )
已知A、B、C、D、E、F、G均为初中化学常见的物质,相互关系如图所示,“→”表示转化关系,“一”表示相互之间能反应(部分反应物、生成物以及反应条件省略).其中,A是人体胃酸的主要成分;B为一种盐;C是一种常用来灭火的气体,过多排放会导致温室效应;D是一种常用的食品干燥剂也可用做建筑材料;组成G单质的元素在地壳中含量居所有金属元素的第二位.分析以上信息及图所示,以下分析错误的是( )| A. | 物质B是可溶性的碳酸盐 | |
| B. | 物质F不可能是可溶性铜盐 | |
| C. | 物质C和D之间说明CO2和CaO在一定条件下能直接反应 | |
| D. | 以上所有物质间的转化可涉及到四个基本反应类型 |
14.2015年世界水日的主题是“水与可持续发展”.下列说法正确的是( )
| A. | 冰水共存物属于纯净物 | |
| B. | 硬水和软水可用石蕊溶液来区分 | |
| C. | 有水生成的反应一定是酸和碱的中和反应 | |
| D. | 水电解时所生成氢气和氧气的质量比为2:1 |
11.下列有关“化学之最”的说法中不正确的是( )
| A. | 空气中含量最多的气体是氮气 | B. | 最轻的气体是氢气 | ||
| C. | 最小的粒子是原子 | D. | 天然存在的最硬的物质是金刚石 |
12.下列物品使用的主要材料,属于有机合成材料的是( )
| A. | 纯棉布袋 | B. | 铝制易拉罐 | C. | 塑料矿泉水瓶 | D. | 纸质蛋糕盒 |