题目内容
18.完成下列表格,根据表格中的信息,总结出四条结论.| 核外电子数 | 相对原 子质量 | |||||
| 名称 | 符号 | 核电荷数 | 质子数 | 中子数 | ||
| 氢 | H | 1 | 1 | 0 | 1 | |
| 氧 | O | 8 | 8 | 8 | 8 | |
| 钠 | Na | 11 | 11 | 11 | 23 | |
| 氯 | Cl | 17 | 17 | 18 | 17 | 35 |
(2)相对原子质量=质子数+中子数.
(3)不同元素质子数不同.
(4)原子内质子数不一定等于中子数.
分析 根据质子数=电子数、相对原子质量=质子数+中子数将表格所缺内容填好,再通过观察数据找出规律性的东西,并能灵活运用
解答 解:由质子数=电子数、相对原子质量=质子数+中子数可知:氢原子的核外电子数是1;氧相对原
子质量是16;钠的中子数是23-11=12.
填好表格内容后,通过观察表格中的数据,我得到了以下启示:在原子中质子数=电子数=核电荷数,相对原子质量=质子数+中子数,不同元素质子数不同,原子内质子数不一定等于中子数,有的原子的原子核中没有中子,但一定有质子等.
| 核外电子数 | 相对原 子质量 | |||||
| 名称 | 符号 | 核电荷数 | 质子数 | 中子数 | ||
| 氢 | H | 1 | 1 | 0 | 1 | |
| 氧 | O | 8 | 8 | 8 | 8 | |
| 钠 | Na | 11 | 11 | 11 | 23 | |
| 氯 | Cl | 17 | 17 | 18 | 17 | 35 |
(1)在原子中质子数=电子数=核电荷数;
(2)相对原子质量=质子数+中子数;
(3)不同元素质子数不同;
(4)原子内质子数不一定等于中子数.
点评 通过回答本题知道了在原子里:质子数=电子数=核电荷数;不同种类的原子,质子数不同;相对原子质量=质子数+中子数.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.在锥形瓶甲中放入10g块状纯净的碳酸钙,在锥形瓶乙中放入10g粉末状纯净的碳酸钙,分别同时加入足量同浓度的稀盐酸与碳酸钙反应.下列图中对该实验产生气体的质量与反应时间的关系,描述合理的是( )
| A. | 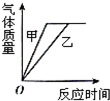 | B. | 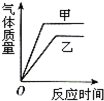 | C. | 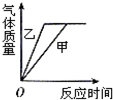 | D. | 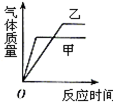 |
13.除去下列括号内杂质,所用试剂及操作错误的是( )
| 物质(杂质) | 所用试剂及操作 | |
| A | 氧化铜(木炭粉) | 在氧气流中加热 |
| B | 氯化亚铁溶液(氯化铜) | 加入足量的铁粉,充分反应后过滤 |
| C | 二氧化锰(氯化钾) | 溶解,过滤,洗涤,烘干 |
| D | 二氧化碳(氯化氢气体) | 通入氢氧化钠溶液,干燥 |
| A. | A | B. | B | C. | C | D. | D |
3.把5.6g含杂质的铁放入足量稀硫酸中,完全反应后放出0.21g氢气,则锌中可能含有的杂质为(只含有一种杂质)( )
| A. | Mg | B. | Al | C. | Zn | D. | Cu |
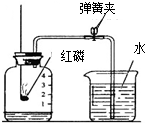 我校某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
我校某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下: