题目内容
6.现有下列物质:①净化后的空气;②二氧化碳;③澄清石灰水;④液态氧;⑤稀有气体;⑥五氧化二磷;⑦蒸馏水;⑧矿泉水;⑨氧化镁;⑩糖水.其中属于混合物的有①③⑤⑧⑩(填序号,下同),属于纯净物的有②④⑥⑦⑨.分析 纯净物是由一种物质组成的物质,混合物是由多种物质组成的物质;据此结合常见物质的组成成分逐项分析即可.
解答 解:①净化后的空气;③澄清石灰水;⑤稀有气体;⑧矿泉水;⑩糖水中都含有多种物质,都属于混合物.
②二氧化碳;④液态氧;⑥五氧化二磷;⑦蒸馏水;⑨氧化镁中都只含有一种物质,都属于纯净物.
故答案为:①③⑤⑧⑩;②④⑥⑦⑨.
点评 解答本题要充分理解纯净物和混合物的区别,要分析物质是由几种物质组成的,如果只有一种物质组成就属于纯净物,如果有多种物质就属于混合物.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.某化学兴趣小组的同学对碳酸钙高温加热一段时间后剩余固体的成分进行探究.
【提出问题】加热后剩余固体的成分是什么?
【猜想与探究】
猜想一:碳酸钙全部溶解,剩余固体成分为氧化钙.
做出该猜想的依据是(用化学方程式表示)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,验证该猜想的方案为把适量固体置于试管中,滴加足量稀盐酸,不产生气泡.
猜想二:碳酸钙部分分解,剩余固体成分为碳酸钙和氧化钙.
验证该猜想的方案如表所示:
【反思与评价】你认为“猜想二”的验证方案存在(填“存在”或“不存在”)问题,理由是氧化钙和水反应生成氢氧化钙,氢氧化钙微溶于水.
【提出问题】加热后剩余固体的成分是什么?
【猜想与探究】
猜想一:碳酸钙全部溶解,剩余固体成分为氧化钙.
做出该猜想的依据是(用化学方程式表示)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,验证该猜想的方案为把适量固体置于试管中,滴加足量稀盐酸,不产生气泡.
猜想二:碳酸钙部分分解,剩余固体成分为碳酸钙和氧化钙.
验证该猜想的方案如表所示:
| 实验步骤 | 实验现象 | 结论 | |
| 步骤A | 将加热后的固体放入水中,搅拌、静置 | 底部有大量白色不溶物 | 剩余固体中含有碳酸钙 |
| 步骤B | 取上层清液 溶液滴加无色 | 变红 | 剩余固体中含有 氧化钙 |
15.下列描述正确的是( )
| A. | 含有不同种元素的物质一定是化合物 | |
| B. | 只有物质和氧气的反应才是氧化反应 | |
| C. | 不同种元素的本质区别是质子数不同 | |
| D. | 金刚石和石墨物理性质差别大的原因是它们的组成结构不同 |
16.用来判断石灰石与稀硫酸反应是化学变化的依据是.
| A. | 固体逐渐减少 | |
| B. | 有气泡产生 | |
| C. | 生成了一种能使澄清石灰水变浑浊的气体 | |
| D. | 所得液体的颜色发生了变化 |

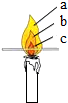 在对蜡烛及其燃烧进行了探究以后,请你填写下列空格:
在对蜡烛及其燃烧进行了探究以后,请你填写下列空格: