题目内容
下列物质露置于空气中,因发生化学变化而使质量增加的是( )
A. 浓硫酸 B. 烧碱溶液 C. 浓盐酸 D. 过氧化氢溶液
某化学小组为了测定学校附近某矿山石灰石碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中的杂质不与稀盐酸反应也不溶于水。)有关实验数据如下表:
反应前 | 反应后 | ||
实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的 质量 | 烧杯和其中混合物质量 |
150g | 12g | 157.6g |
(1)根据质量守恒定律,反应中生成二氧化碳的质量为______g.
(2)求该石灰石样品中碳酸钙的质量_____。
实验室可利用碱式碳酸铜(化学式:Cu2(OH)2CO3)制备氧化铜,并进行碳粉还原氧化铜的实验。
查阅资料:烧碱固体有吸水性且能与二氧化碳发生反应。
无水硫酸铜遇水会由白色变成蓝色。
①制备氧化铜并检验产物,装置如图所示(省略夹持仪器):
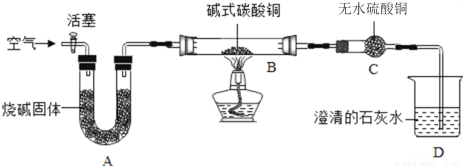
步骤一:连接A和B,打开活塞,通入空气。
步骤二:关闭活塞,连上C和D开始加热。观察到C中固体变蓝,D中澄清石灰水变浑浊。
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热。
加热时间(min) | 0 | t1 | t2 | t3 |
B中固体质量(g) | 6.66 | 5.20 | 4.80 | 4.80 |
①B中发生反应的化学方程式为:__________ , A的作用是吸收空气中的_______ ,防止对产物检验造成干扰。选择t3时停止加热的理由是____________。
②一定量碳粉还原①中制得的氧化铜并检验产物,装置如图所示:写出该反应的化学方程式________,实验过程中,观察到F中溶液变浑浊,E中的现象是___________ 反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是____________

③若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因______________。
④计算②反应后理论上可制得多少克铜__________。



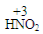 (亚硝酸)
(亚硝酸)