题目内容
 小美同学打算用金属的置换反应制取氢气.请问:
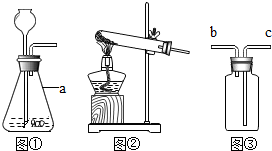
小美同学打算用金属的置换反应制取氢气.请问:(1)她绘出如图表示的制取氢气的装置,该图有哪些错误,怎样改进?
(2)她改正装置后,用镁和铝从稀硫酸中置换出氢气.若分别用等质量的镁和铝与足量稀硫酸反应,制得的氢气的质量比是多少?
(3)请你设计利用锌粒跟稀硫酸反应制备氢气的装置,要求该装置能方便地控制反应进行或停止.画出其装置示意图.
考点:氢气的制取和检验,金属的化学性质
专题:金属与金属材料
分析:根据实验中常见装置的注意事项可填空,一般情况下长颈漏斗下端管要浸入酸液中,导气管应刚露出试管塞为宜;向下排空气法收集时导气管伸入集气瓶底部,根据“用等质量的镁和铝与足量稀硫酸反应”,则根据氢气的质量=
×金属质量进行分析.
| 金属的化合价 |
| 金属的相对原子质量 |
解答:解:
(1)①图中没有用长颈漏斗,且下端没有伸入到锥形瓶内液面以下;为防止气体跑出,应该把长颈漏斗下端伸入到锥形瓶内液面以下,起到液封的目;
②装置左边试管中的导管太长,不能导出气体,应只露出橡皮塞即可;
③导气管伸入集气瓶过短,会影响气体的收集,应伸入集气瓶底部,并且需要向下排空气法收集;
(2)根据“用等质量的镁和铝与足量稀硫酸反应”,则根据氢气的质量=
×金属质量,假设等质量的镁和铝都为1g,则它们与足量稀硫酸反应生成氢气的质量分别为
g、
g,故制得的氢气的质量比是
g:
g=3:4;
(3)图中装置通过打开或关闭止水夹能改变装置内的压强,使固体和液体药品接触或分开,从而达到控制反应的发生或停止的目的,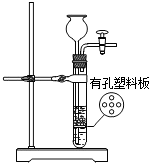 .
.
故答案为:
(1)①图中没有用长颈漏斗,且下端没有伸入到锥形瓶内液面以下;为防止气体跑出,应该把长颈漏斗下端伸入到锥形瓶内液面以下,起到液封的目;
②装置左边试管中的导管太长,不能导出气体,应只露出橡皮塞即可;
③导气管伸入集气瓶过短,会影响气体的收集,应伸入集气瓶底部,并且需要向下排空气法收集;
(2)3:4;
(3) .
.
(1)①图中没有用长颈漏斗,且下端没有伸入到锥形瓶内液面以下;为防止气体跑出,应该把长颈漏斗下端伸入到锥形瓶内液面以下,起到液封的目;
②装置左边试管中的导管太长,不能导出气体,应只露出橡皮塞即可;
③导气管伸入集气瓶过短,会影响气体的收集,应伸入集气瓶底部,并且需要向下排空气法收集;
(2)根据“用等质量的镁和铝与足量稀硫酸反应”,则根据氢气的质量=
| 金属的化合价 |
| 金属的相对原子质量 |
| 2 |
| 24 |
| 3 |
| 27 |
| 2 |
| 24 |
| 3 |
| 27 |
(3)图中装置通过打开或关闭止水夹能改变装置内的压强,使固体和液体药品接触或分开,从而达到控制反应的发生或停止的目的,
 .
.故答案为:
(1)①图中没有用长颈漏斗,且下端没有伸入到锥形瓶内液面以下;为防止气体跑出,应该把长颈漏斗下端伸入到锥形瓶内液面以下,起到液封的目;
②装置左边试管中的导管太长,不能导出气体,应只露出橡皮塞即可;
③导气管伸入集气瓶过短,会影响气体的收集,应伸入集气瓶底部,并且需要向下排空气法收集;
(2)3:4;
(3)
 .
.点评:要熟记实验室制取氢气的反应原理、实验步骤、装置示意图及其中仪器的名称、实验注意事项,以及氢气的检验.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
下列说法错误的是( )
| A、有氧气反应一定是氧化反应 |
| B、催化剂一定加快反应速率 |
| C、混合物中一定有多种物质 |
| D、化学变化中一定有物理变化 |