题目内容
12.以下是研究实验室制取氧气的装置图,请按要求回答下列问题.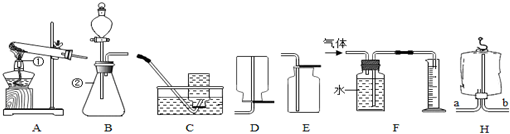
(1)写出图中标号仪器的名称:①酒精灯;②锥形瓶.
(2)实验室用氯酸钾制取氧气,应选用的发生装置是A(填字母序号,下同),若要收集一瓶干燥的A氧气,应选择的收集装置是E.该反应的文字表达式是:氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气.
在加热氯酸钾制取氧气的过程中,发现产生氧气的速率很慢,经检查不是氯酸钾变质,也不是装置气密性不好,你认为最可能的原因是:没添加二氧化锰
(3)实验室用过氧化氢溶液和二氧化锰混合制氧气,其中二氧化锰起催化作用,该反应的文字表达式为:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气
同学们利用B和F装置,通过排水量来测定生成氧气的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值偏大(水的体积测量准确),其主要原因是当双氧水从分液漏斗中流入锥形瓶时,会将锥形瓶中的一部分空气排出并进入F装置,导致量筒内收集到的水的体积总是比理论值大得多
(4)若用图H所示医用塑料袋排空气法收集氢气,则氢气导入端为b(填“a”或“b”)
(5)若收集一瓶氧气,供硫粉在氧气中燃烧的实验使用,最好选用气体的收集装置中的C(填装置序号),理由是:硫燃烧生成的二氧化硫有毒,且能溶于水,所以可在集气瓶中放一些水进行吸收,防止污染大气,利用排水法收集氧气便于在瓶中留一些水
(6)已知一氧化氮气体难溶于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中装置C(填字母序号),说明一氧化氮已收集满的现象是有气泡从集气瓶口冒出.
分析 (1)熟练掌握常见化学仪器的名称及其用途;
(2)加热氯酸钾制取氧气,发生装置的特点属于固体加热型;排空气法收集的气体较干燥,排水法收集的氧气较纯净;根据反应物、生成物书写反应的文字表达式;根据
氯酸钾分解速率慢的原因分析;
(3)实验室用H2O2溶液和MnO2混合制氧气,二氧化锰是催化剂,改变了过氧化氢溶液的分解速率;根据反应物、生成物书写反应的文字表达式;根据实验的流程及注意事项分析;
(4)根据氢气的密度选择进气口;
(5)根据硫燃烧生成的二氧化硫有毒,且能溶于水,所以可在集气瓶中放一些水进行吸收,防止污染大气,利用排水法收集氧气便于在瓶中留一些水进行分析;
(6)根据一氧化氮的密度和溶解性选择收集装置,并据排水法收集气体分析解答.
解答 解:(1)①是酒精灯; ②是锥形瓶;
(2)加热氯酸钾和二氧化锰的混合物制取氧气,发生装置的特点属于固体加热型的A装置;因为氧气不易溶于水且密度大于空气,所以既可以用排水法收集,也可以用向上排空气法收集;排水法收集的气体较纯,而向上排空气法收集的气体较干燥;反应的文字表达式为:氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气;氯酸钾分解速率慢的原因可能是没有添加二氧化锰或二氧化锰的量很少;
(3)实验室用H2O2溶液和MnO2混合制氧气,二氧化锰是催化剂,改变了过氧化氢溶液的分解速率,起到催化作用;反应的文字表达式为:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;量筒内收集到的水的体积总是比理论值偏大主要原因可能是:当双氧水从分液漏斗中流入锥形瓶时,会将锥形瓶中的一部分空气排出并进入F装置,导致量筒内收集到的水的体积总是比理论值大得多.
(4)因为氢气的密度比空气小,故氢气从长管进入到医用塑料袋的上方,把空气从短管排出;
(5)硫燃烧生成的二氧化硫有毒,且能溶于水,所以可在集气瓶中放一些水进行吸收,防止污染大气,利用排水法收集氧气便于在瓶中留一些水;
(6)一氧化氮气体难溶于水,在空气中容易与氧气发生反应,所以只能用排水法收集,说明一氧化氮已收集满的现象是有气泡从集气瓶口冒出.
故答案为:(1)酒精灯;锥形瓶;
(2)A;E,氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气;没添加二氧化锰;
(3)催化;过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;当双氧水从分液漏斗中流入锥形瓶时,会将锥形瓶中的一部分空气排出并进入F装置,导致量筒内收集到的水的体积总是比理论值大得多;
(4)b;
(5)C;硫燃烧生成的二氧化硫有毒,且能溶于水,所以可在集气瓶中放一些水进行吸收,防止污染大气,利用排水法收集氧气便于在瓶中留一些水;
(6)C;有气泡从集气瓶口冒出.
点评 本题考查了常见气体氧气的制取装置、收集方法的选择及实验误差的分析、二氧化碳的性质探究,可以根据制取气体发生装置、收集装置选择的依据结合实验的现象和结论逐一分析.

 阅读快车系列答案
阅读快车系列答案 ”、“
”、“ ”、“
”、“ ”分别表示A、B、C三种物质的分子,如图形象地表示了某化学反应前后反应物与生成物分子及其数目的变化.则该反应的化学方程式中A、B、C前的化学计量数之比为( )
”分别表示A、B、C三种物质的分子,如图形象地表示了某化学反应前后反应物与生成物分子及其数目的变化.则该反应的化学方程式中A、B、C前的化学计量数之比为( )
| A. | 3:2:4 | B. | 1:2:2 | C. | 1:2:3 | D. | 3:2:2 |
| A. | 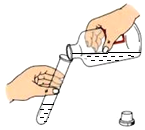 液体的倾倒 | B. | 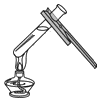 液体的加热 | ||
| C. | 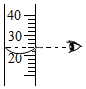 量取一定量的液体 | D. | 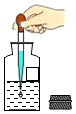 用滴管取液体 |
| A. | 逐滴加入较稀的双氧水 | B. | 加水稀释 | ||
| C. | 减少双氧水的用量 | D. | 升高温度 |