题目内容
我国属于海洋大国,浩瀚的海域蕴藏着丰富的化学资源.
(1)海底蕴藏着大量的煤、 、天然气等常规化石燃料.
(2)天然气的主要成分是甲烷(CH4),可直接用作气体燃料.燃烧反应前后分子种类变化的微观示意图如图1所示.

①1个A分子中含有 个原子.
②四种物质中属于单质的是 (填图中字母).
(3)海水晒盐能够得到粗盐和卤水.卤水中含有MgCl2、KCl和MgSO4等物质,图2是它们的溶解度曲线.t1℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液中,溶质质量分数最大的是 .将t1℃的MgCl2、KCl和MgSO4三种物质的饱和溶液加热到t2℃以上时,可能会析出 晶体.
(1)海底蕴藏着大量的煤、
(2)天然气的主要成分是甲烷(CH4),可直接用作气体燃料.燃烧反应前后分子种类变化的微观示意图如图1所示.

①1个A分子中含有
②四种物质中属于单质的是
(3)海水晒盐能够得到粗盐和卤水.卤水中含有MgCl2、KCl和MgSO4等物质,图2是它们的溶解度曲线.t1℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液中,溶质质量分数最大的是
考点:化石燃料及其综合利用,固体溶解度曲线及其作用,晶体和结晶的概念与现象,溶质的质量分数、溶解性和溶解度的关系,微粒观点及模型图的应用
专题:化学反应模拟图型,化学与能源,溶液、浊液与溶解度
分析:(1)根据化石能源的种类分析回答;
(2)根据微粒的构成分析分子的构成、物质的类别;
(3)根据饱和溶液的质量分数的影响因素和降温后溶解度的变化考虑.
(2)根据微粒的构成分析分子的构成、物质的类别;
(3)根据饱和溶液的质量分数的影响因素和降温后溶解度的变化考虑.
解答:解:(1)海底蕴藏着大量的煤、石油、天然气等常规化石燃料;
(2)由微粒的构成可知:①1个A分子中含有4个原子.
②四种物质中.B的分子是由同种的原子构成的,属于单质.
(3)由饱和溶液溶质质量分数于溶解度的关系可知,溶解度大的,溶质质量分数就大,所以t1℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液中,溶质质量分数最大的是氯化镁;将t1℃的MgCl2、KCl和MgSO4三种物质的饱和溶液升温至t2℃时,只要溶解度减小的就能析出晶体,由图示可知MgSO4的溶解度变小,能析出晶体.
故答为:(1)石油;(2)①4;②B;(3)MgCl2,MgSO4.
(2)由微粒的构成可知:①1个A分子中含有4个原子.
②四种物质中.B的分子是由同种的原子构成的,属于单质.
(3)由饱和溶液溶质质量分数于溶解度的关系可知,溶解度大的,溶质质量分数就大,所以t1℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液中,溶质质量分数最大的是氯化镁;将t1℃的MgCl2、KCl和MgSO4三种物质的饱和溶液升温至t2℃时,只要溶解度减小的就能析出晶体,由图示可知MgSO4的溶解度变小,能析出晶体.
故答为:(1)石油;(2)①4;②B;(3)MgCl2,MgSO4.
点评:本题的第三题稍有难度,解答本题关键要溶解度的意义,了解饱和溶液溶质质量分数的影响因素,饱和溶液降温后,只要溶解度减小就会析出晶体.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案
相关题目
逻辑推理是化学学习常用的思维方法,下列推理正确的是( )
| A、单质是含一种元素的物质,则含一种元素的物质就是单质 |
| B、原子在化学变化中不能再分,则分子在化学变化中也不能再分 |
| C、点燃H2与O2混合气体可能爆炸,则点燃H2要检验纯度 |
| D、氧化物都含有氧元素,所以含有氧元素的化合物都是氧化物 |
下列操作不正确的是( )
| A、用燃烧的木条鉴别氢气、氧气和二氧化碳 |
| B、用磷在密闭容器中燃烧,除去密闭容器内空气中的氧气 |
| C、生活中为了降低水的硬度往往采用加热煮沸的方法 |
| D、用KMnO4制氧气时,应先熄灭酒精灯再从水槽中撤出导管 |
某些金属工艺品的外观有银白色的金属光泽,同学们认为它可能和铁一样,有磁性.在讨论时,有的同学提出“我们可以拿磁铁来吸引一下”.“拿磁铁来吸引一下”这“言论,属于科学探究中的( )
| A、假设 | B、设计实验 |
| C、观察 | D、得出结论 |
除去CO中混入的少量CO2,可采用的方法是( )
| A、把混合气体点燃 |
| B、把混合气体通过足量的澄清石灰水 |
| C、把混合气体通过灼热的CuO |
| D、把混合气体从一个容器倾倒到另一个容器中 |
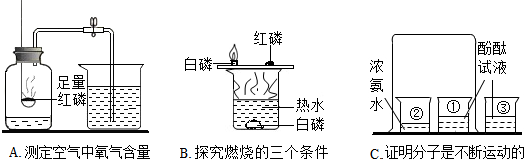
 某同学用图所示装置来测定空气中氧气的体积分数,请填写下列空白.
某同学用图所示装置来测定空气中氧气的体积分数,请填写下列空白.