题目内容
13.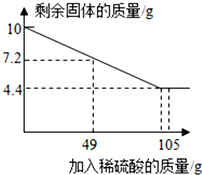 湿法炼铜化学反应方程式为Fe+CuSO4═FeSO4+Cu现称取10克铜、铁混合物置于烧杯中,滴加一定质量分数的稀硫酸溶液,记录并绘制如图所示的曲线.
湿法炼铜化学反应方程式为Fe+CuSO4═FeSO4+Cu现称取10克铜、铁混合物置于烧杯中,滴加一定质量分数的稀硫酸溶液,记录并绘制如图所示的曲线.①10克固体混合物中铜的质量为4.4 g.
②所用稀硫酸溶液溶质的质量分数是多少?
分析 根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可
①根据图示数据可知最后加入硫酸后固体质量不再减少,说明剩余的物质都是铜,再进行计算;
②根据铁的质量结合化学方程式计算出消耗硫酸的质量,根据溶质质量分数的公式解答即可.
解答 解:湿法炼铜是利用了铁与硫酸铜溶液发生置换反应,生成硫酸亚铁溶液和铜,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu.
①根据图示数据可知最后加入硫酸后固体质量不再减少,说明剩余的物质都是铜,10克固体混合物中铜的质量为4.4g;
②根据图中数据可知,加入49g稀硫酸时消耗铁的质量是10g-7.2g=2.8g,设49g稀硫酸中溶质的质量为x,
Fe+H2SO4═FeSO4+H2↑
56 98
2.8g x
$\frac{56}{2.8g}=\frac{98}{x}$
x=4.9g
所用稀硫酸溶液溶质的质量分数是:$\frac{4.9g}{49g}×100%$=10%;
答案:Fe+CuSO4═FeSO4+Cu.
①4.4g;
②所用稀硫酸溶液溶质的质量分数是10%.
点评 解答本题关键是要分析出加入硫酸后固体质量不再减少,说明剩余的物质都是铜.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.如图为某化学反应的微观示意图,其中不同的球代表不同种原子.下列说法中正确的是( )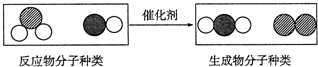

| A. | 此反应属于置换反应 | |
| B. | 化学反应前后分子的种类没有改变 | |
| C. | 原子在化学变化中可分 | |
| D. | 参加反应的两种分子的个数比为1:2 |
4.下列四个图象分别对应四个变化过程的一种趋势,其说法正确的是( )
?①表示在等质量的铁粉和锌粉中分别加入足量的溶质质量分数相等的稀硫酸
?②用加热一定质量的氯酸钾和二氧化锰固体混合物的方法制取氧气
?③向一定量的硫酸和硫酸铜的混合溶液中逐滴加入一定质量分数的氢氧化钠溶液
④向一定量的氢氧化钠溶液中加水稀释,溶液的pH变化
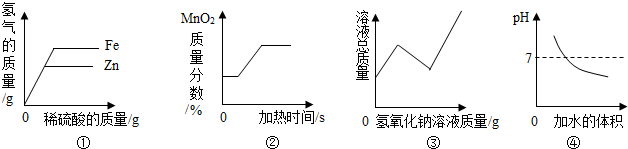
?①表示在等质量的铁粉和锌粉中分别加入足量的溶质质量分数相等的稀硫酸
?②用加热一定质量的氯酸钾和二氧化锰固体混合物的方法制取氧气
?③向一定量的硫酸和硫酸铜的混合溶液中逐滴加入一定质量分数的氢氧化钠溶液
④向一定量的氢氧化钠溶液中加水稀释,溶液的pH变化

| A. | 上述图象只有2个正确 | |
| B. | 上述图象只有3个正确 | |
| C. | 上述图象全部正确 | |
| D. | 如果将②中的纵坐标改为固体总质量,该图象能正确反映相应的变化趋势 |
1.蔗糖的化学式为(C12H22O11),它是食品中常用的甜味剂,下列有关说法正确的是( )
| A. | 蔗糖属于无机化合物 | |
| B. | 蔗糖中氢元素的质量分数最大 | |
| C. | 一个蔗糖分子中有45个原子构成 | |
| D. | 蔗糖中碳、氢、氧元素的质量比为12:22:11 |
8.(1)请在表中填入一种相应的物质的化学式:
(2)用上表的四种具体物质为反应物,写出两个它们之间相互反应的化学方程式:
①Fe+2HCl=FeCl2+H2↑;②HCl+NaOH=NaCl+H2O.
| 类别 | 单质 | 酸 | 碱 | 盐 |
| 化学式 |
①Fe+2HCl=FeCl2+H2↑;②HCl+NaOH=NaCl+H2O.
3.下列分类正确的是( )
| A. | 金刚石、黄金:金属单质 | B. | 合金和合成橡胶:合成材料 | ||
| C. | 干冰、生石灰:氧化物 | D. | 烧碱和纯碱:碱 |
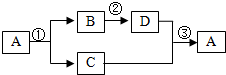
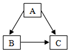 化合物A、B、C都含三种元素,其中两种元素的质量比均为1:2.它们之间有如图所示的关系,在图示的三个化学反应中(“→”表示转化关系):一个反应有沉淀生成,另一个反应有气体生产,还有一个反应既有沉淀又有水生成.请回答下列问题:
化合物A、B、C都含三种元素,其中两种元素的质量比均为1:2.它们之间有如图所示的关系,在图示的三个化学反应中(“→”表示转化关系):一个反应有沉淀生成,另一个反应有气体生产,还有一个反应既有沉淀又有水生成.请回答下列问题: