题目内容
12.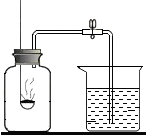 某同学用如图装置测定空气中氧气的体积分数.请你填写有关空格,并与同学交流.
某同学用如图装置测定空气中氧气的体积分数.请你填写有关空格,并与同学交流.(1)该实验中,红磷需稍过量,目的是尽可能把氧气反应掉.该物质燃烧反应的表达式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)待该物质熄灭并冷却后,打开弹簧夹观察到的现象是水经导气管流向集气瓶中约五分之一体积处;出现该现象的原因是由于磷燃烧消耗了氧气使瓶内压强减小,小于外界大气压;为什么要“待该物质熄灭并冷却后,打开弹簧夹”?使实验结果准确
(3)实验后发现测定出的空气中氧气的体积分数低于$\frac{1}{5}$,这可能是由哪几种原因引起的?没有冷却至室温,就打开弹簧夹;装置气密性不够好;红磷量不足;集气瓶中的氧气没有消耗完
(4)若(3)实验后发现测定出的空气中氧气的体积分数大于$\frac{1}{5}$,这可能是由哪几种原因引起的?燃烧的红磷刚插入集气瓶时没有塞紧,燃烧一段时间后再塞紧;没有先用弹簧夹夹紧橡皮管;导气管中的氧气参与了反应等
(5)由本实验还可以推测氮气的性质有难溶于水.
(6)若将红磷换成碳粉,该实验能否获得成功?否(填能或否)理由是由于碳粉燃烧的产物是二氧化碳气体,瓶内气压没变,水不能进入集气瓶.
分析 (1)为了使实验结果准确,要用过量的红磷确保氧气被完全消耗掉;该反应生成了五氧化二磷,可以据此写出该反应的文字表达式;
(2)根据磷燃烧消耗氧气使瓶内压强减小来分析;
(3)根据可能造成进入水的体积少的原因进行分析;
(4)测定出的空气中氧气的体积分数大于五分之一即从瓶中出来一些气体,再分析具体原因;
(5)对比氧气和环境来具体分析氮气的性质.
(6)根据反应原理进行分析.
解答 解:(1)该实验中,红磷需稍过量,目的是 尽可能把氧气反应掉.红磷在空气中燃烧,其实质上是与空气中的氧气反应生成五氧化二磷,其反应的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)由于磷燃烧消耗了氧气使瓶内压强减小,小于外界大气压,在外界大气压的作用下,把水压入瓶内,由于水进入瓶内的体积约占瓶子总体积的五分之一,所以结论是氧气约占空气体积的五分之一;待该物质熄灭并冷却后,打开弹簧夹是实验结果准确;
(3)造成进入水的体积少的原因:装置漏气、红磷量不足没有把瓶内氧气消耗完,没有冷却到室温就打开了止水夹;
(4)测定出的空气中氧气的体积分数大于五分之一
即从瓶中出来一些气体,由于磷燃烧放热,由于集气瓶的瓶塞没有塞紧,瓶内空气有部分被赶了出来;或者没有先用弹簧夹夹紧橡皮管,磷燃烧时有部分空气沿着导管出来了;
(5)氮气的性质的归纳,要从本实验的实际来进行,不要脱离题目去回答和分析.实验中当装置内进入水以后,氮气依然能够存在这就说明氮气是难溶于水的也不和水反应.另外在红磷和氧气反应的过程中,氮气没有被消耗,所以氮气不和氧气、红磷反应,可以概括为性质稳定,当然也可以分开叙述,就是不和氧气反应,不支持燃烧等.
(6)否;由于碳粉燃烧的产物是二氧化碳气体,瓶内气压没变,水不能进入集气瓶.
故答案为:
(1)尽可能把氧气反应掉.4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)水经导气管流向集气瓶中约五分之一体积处;由于磷燃烧消耗了氧气使瓶内压强减小,小于外界大气压;使实验结果准确;
(3)没有冷却至室温,就打开弹簧夹;装置气密性不够好;红磷量不足;集气瓶中的氧气没有消耗完;
(4)燃烧的红磷刚插入集气瓶时没有塞紧,燃烧一段时间后再塞紧;没有先用弹簧夹夹紧橡皮管;导气管中的氧气参与了反应等;(合理即可);
(5)难溶于水;
(6)否;生成物二氧化碳是气体,瓶内气压没有改变.
点评 本题以空气中氧气的含量为载体,考查了相关化学方程式的书写、所测氧气含量偏低的原因、氮气的性质等,考查学生科学探究和逻辑思维的能力.

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案| A. | 一定条件下,SO2和O2生成SO3,反应前后分子总数不变 | |
| B. | 煤燃烧后剩余残渣的质量减轻了 | |
| C. | 1克的氢气和1克的氧气完全燃烧,后生成2克的水 | |
| D. | 某有机物在空气中燃烧只生成CO2和H2O,则该有机物一定含有碳、氢、氧元素 |
| A. | 从燃烧条件看,纸尿裤属于可燃物 | |
| B. | 火灾发生后要立即拨打“119” | |
| C. | 水枪灭火时因为水降低了纸尿裤的着火点 | |
| D. | 存放纸尿裤等易燃物时不可堆得过密 |
| A. | 碳能形成多种单质,如:金刚石、石墨、C60等.碳具有还原性,用焦炭可冶炼铁 | |
| B. | SO3、CO2、CO是非金属氧化物,都可用NaOH溶液吸收 | |
| C. | C、CO、CH4、C2H2OH均能作为燃料使用 | |
| D. | 铁是化学性质比较活泼的金属,除与氧气反应外,还能与某些酸和盐溶液发生置换反应 |
| A. | CO2 | B. | O2 | C. | 2O2 | D. | 2O |
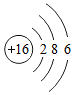 所表示的粒子符号为S,在化学反应中易得到电子(填“得到”或“失去”).
所表示的粒子符号为S,在化学反应中易得到电子(填“得到”或“失去”).