题目内容
11.下列各物质中,前者属于混合物,后者属于化合物的是( )| A. | 稀硫酸 酒精 | B. | 石灰水 铁粉 | C. | 空气 稀盐酸 | D. | 海水 氮气 |
分析 根据混合物与纯净物的特点分析:混合物是由多种物质组成的物质;化合物是由不同种元素组成的纯净物.
解答 解:A、稀硫酸中含有水和硫酸,属于混合物;酒精是由不同种元素组成的纯净物,属于化合物;
B、石灰水中含有水和氢氧化钙,属于混合物;铁是由一种元素组成的纯净物,属于单质;
C、空气中含有氮气、氧气等物质,属于混合物;稀盐酸中含有水和氯化氢,属于混合物;
D、海水中含有多种物质,属于混合物;氮气是由一种元素组成的纯净物,属于单质.
故选A.
点评 本题主要考查物质的分类方法,解答时要分析物质的元素组成和物质组成,然后再根据各类物质概念的含义进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
11.日常生活中接触的下列物质,能使紫色石蕊溶液变蓝的是( )
| A. | 酸奶 | B. | 食盐 | C. | 蔗糖水 | D. | 肥皂水 |
3.某学习小组对粗盐中杂质(难溶性和可溶性)的去除展开相关探究.
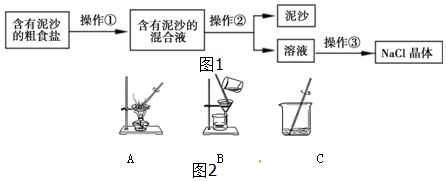
(1)粗盐中难溶性杂质去除的实验步骤为:①溶解,②过滤,③蒸发(写操作名称),④计算产率.
(2)步骤②中需要用到的玻璃仪器有:玻璃棒、烧杯、漏斗(写仪器名称),其中玻璃棒的作用是引流.
(3)【提出猜想】
该粗盐中含有难溶性杂质外,是否还含有可溶性杂质?
(4)【查阅资料】
①粗盐中可能含有镁盐(Mg2+)和硫酸盐(SO42-)等可溶性杂质.
②一些物质的溶解性表
说明:“溶”表示该物质可溶于水,“不”表示该物质不溶于水.
③Mg(OH)2为白色物质,不溶于氢氧化钠溶液;BaSO4为白色物质,不溶于盐酸;
MgCO3,BaCO3为白色物质都能溶于盐酸.
(5)【实验设计】
①取少量除去难溶性杂质后的盐,溶于水配成溶液.
②取少量所配溶液于试管中,滴加氢氧化钠溶液,产生白色沉淀,继续滴加氢氧化钠溶液,沉淀不溶,说明该盐含有可溶性的镁盐.
③另取少量所配溶液于试管中,滴加氯化钡溶液,产生白色沉淀,再加稀盐酸,沉淀不溶,说明该盐含有可溶性的硫酸盐.
(6)【实验结论】该盐含有可溶性杂质硫酸镁.其与氢氧化钠溶液反应的化学方程式为2NaOH+MgSO4═Na2SO4+Mg(OH)2↓.
(1)粗盐中难溶性杂质去除的实验步骤为:①溶解,②过滤,③蒸发(写操作名称),④计算产率.
(2)步骤②中需要用到的玻璃仪器有:玻璃棒、烧杯、漏斗(写仪器名称),其中玻璃棒的作用是引流.
(3)【提出猜想】
该粗盐中含有难溶性杂质外,是否还含有可溶性杂质?
(4)【查阅资料】
①粗盐中可能含有镁盐(Mg2+)和硫酸盐(SO42-)等可溶性杂质.
②一些物质的溶解性表
| 阳离子 阴离子 | OH- | Cl- | SO42- | CO32- |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 不 | 不 |
| Mg2+ | 不 | 溶 | 溶 | 不 |
③Mg(OH)2为白色物质,不溶于氢氧化钠溶液;BaSO4为白色物质,不溶于盐酸;
MgCO3,BaCO3为白色物质都能溶于盐酸.
(5)【实验设计】
①取少量除去难溶性杂质后的盐,溶于水配成溶液.
②取少量所配溶液于试管中,滴加氢氧化钠溶液,产生白色沉淀,继续滴加氢氧化钠溶液,沉淀不溶,说明该盐含有可溶性的镁盐.
③另取少量所配溶液于试管中,滴加氯化钡溶液,产生白色沉淀,再加稀盐酸,沉淀不溶,说明该盐含有可溶性的硫酸盐.
(6)【实验结论】该盐含有可溶性杂质硫酸镁.其与氢氧化钠溶液反应的化学方程式为2NaOH+MgSO4═Na2SO4+Mg(OH)2↓.
20.下列关于金属资源的说法中,不正确的是( )
| A. | 地球上除少数不活泼的金属如金、银等有单质形式存在外,其余都以化合物形式存在 | |
| B. | 合理开采矿物、寻找金属代替品都是保护金属资源的有效途径 | |
| C. | 防止金属腐蚀、回收利用废旧金属可以保护金属资源和环境 | |
| D. | 地球上的金属资源是取之不尽的 |
1.下列化合物中,属于有机物的是( )
| A. | 盐酸 | B. | 碳酸 | C. | 醋酸 | D. | 硫酸 |