题目内容
3.实验室制取气体的发生装置和收集装置如图所示(答装置时用字母填空):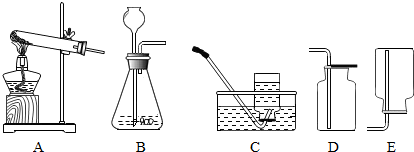
(1)实验室可用发生装置A制取氧气,选取的理由是药品是固体,且反应需要加热,其中发生的一个反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;可用收集装置C收集氧气是因为氧气不易溶于水.用C收集到的氧气不纯,其可能的原因之一是集气瓶没有装满水或没有等到气泡连续、均匀冒出就收集;检验氧气的操作方法是将带火星的木条伸入集气瓶中,木条复燃,证明是氧气.
(2)实验室制取二氧化碳的反应原理是CaCO3+2HCl=CaCl2+H2O+CO2↑(用化学方程式表示),选用的装置为BD.
(3)实验室可用发生装置A和B制取氧气,B相对于A的优点之一是节能或便于添加药品.
(4)收集装置D中,导管口之所以要接近集气瓶底部是为了快速排净集气瓶中的空气.
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;氧气的检验方法是:将带火星的木条伸入集气瓶中,木条复燃,证明是氧气.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.用C收集到的氧气不纯,其可能的原因之一是:集气瓶没有装满水或没有等到气泡连续、均匀冒出就收集;B相对于A的优点是:节能或便于添加药品;收集装置D中,导管口之所以要接近集气瓶底部是为了快速排净集气瓶中的空气.
解答 解:(1)实验室可用发生装置A制取氧气,选取的理由是:药品是固体,且反应需要加热;如果用高锰酸钾或氯酸钾制氧气就需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;用C收集到的氧气不纯,其可能的原因之一是:集气瓶没有装满水或没有等到气泡连续、均匀冒出就收集;氧气的检验方法是:将带火星的木条伸入集气瓶中,木条复燃,证明是氧气;故答案为:药品是固体,且反应需要加热;2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;氧气不易溶于水;集气瓶没有装满水或没有等到气泡连续、均匀冒出就收集;将带火星的木条伸入集气瓶中,木条复燃,证明是氧气;
(2)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;BD;
(3)B相对于A的优点是:节能或便于添加药品;故答案为:节能或便于添加药品;
(4)收集装置D中,导管口之所以要接近集气瓶底部是为了快速排净集气瓶中的空气,故答案为:快速排净集气瓶中的空气;
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的检验和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

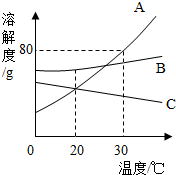 如图是A、B、C 三种物质的溶解度曲线,下列分析错误的是( )
如图是A、B、C 三种物质的溶解度曲线,下列分析错误的是( )| A. | 30℃时,A物质的溶解度最大 | |
| B. | 升温可使C物质的不饱和溶液变成饱和溶液 | |
| C. | 30℃时,把50gA物质放入50g水中能得到100g溶液 | |
| D. | 20℃时,B物质饱和溶液的溶质质量分数最大 |
| A. | 太阳能、风能、核能、氢能都属于新能源 | |
| B. | 空气是人类宝贵的自然资源,其中含量最多的是N2 | |
| C. | 石油经加热炼制,可得到汽油、煤焦油、柴油等不同产品 | |
| D. | 金属资源是有限的,要加强废旧金属的回收和再利用 |
| A. | 其摩尔质量为74 | |
| B. | 其中硫元素的质量分数最大 | |
| C. | 该成分中碳、氢、硫原子的物质的量之比为3:6:1 | |
| D. | 该物质共由10个原子构成 |
 (1)20℃时,A、B、C三种物质的溶解度由大到小顺序是B>A>C.
(1)20℃时,A、B、C三种物质的溶解度由大到小顺序是B>A>C.