题目内容
将H2和O2的混合气体15g,充分燃烧后得到9g水,则反应前的混合气体中最少含有氢气 g,最多含有氢气 g.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据氢气在氧气中燃烧生成水,由生成水的质量根据反应的化学方程式可计算出参加反应的氢气和氧气的质量,据此进行分析解答.
解答:解:设参加反应生成的氢气的质量为x,
2H2+O2
2H2O
4 36
x 9g
=
x=1g
则参加反应的氧气的质量为9g-1g=8g
若混合气体反应后氧气有剩余,则反应前的混合气体中最少含有氢气为1g.
若混合气体反应后氢气有剩余,则反应前的混合气体中最多含有氢气1g+15g-9g=7g.
故答案为:1;7.
2H2+O2
| ||
4 36
x 9g
| 4 |
| 36 |
| x |
| 9g |
则参加反应的氧气的质量为9g-1g=8g
若混合气体反应后氧气有剩余,则反应前的混合气体中最少含有氢气为1g.
若混合气体反应后氢气有剩余,则反应前的混合气体中最多含有氢气1g+15g-9g=7g.
故答案为:1;7.
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意反应后气体的组成成分.

练习册系列答案
相关题目
下列有关实验现象的描述正确的是( )
| A、碳在氧气中燃烧放出白烟 |
| B、红磷在空气中燃烧出现大量的白雾 |
| C、铁丝在氧气中燃烧生成四氧化三铁 |
| D、硫在氧气中燃烧发出蓝紫色火焰 |
某合金60g与足量的稀盐酸完全反应,生成2g氢气,则该合金可能是( )
| A、Fe和Zn |
| B、Mg和Al |
| C、Mg和Fe |
| D、Fe和Cu |
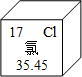 元素周期表是学习和研究化学的重要工具,元素周期表中的氯元素,下列说法不正确的是( )
元素周期表是学习和研究化学的重要工具,元素周期表中的氯元素,下列说法不正确的是( )| A、氯元素符号为Cl |
| B、氯元素为金属元素 |
| C、氯原子的核内质子数为17 |
| D、氯元素的相对原子质量为35.5 |
日常生活中,与肥皂水作用容易起泡沫的是( )
| A、长江水 |
| B、矿泉水 |
| C、煮沸的水 |
| D、含较多可溶性钙、镁化合物的水 |
 如图是实验室制取氧气的实验装置图,按下列要求填写内容.
如图是实验室制取氧气的实验装置图,按下列要求填写内容.