题目内容
15.取氯化钠和碳酸钠的固体混合物16.9g,加入55.5g盐酸恰好与其完全反应,放出4.4g气体,并形成20℃的饱和溶液求:(1)盐酸溶液中溶质的质量分数;(2)反应后所得溶液中溶质的质量分数.
分析 碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳,由生成二氧化碳的质量,由反应的化学方程式列式计算出盐酸溶液中溶质的质量、生成氯化钠的质量,进而计算出溶质的质量分数.
解答 解:设盐酸溶液中溶质的质量为x,生成氯化钠的质量为y,参加反应的碳酸钠的质量为z,
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
z x y 4.4g
(1)$\frac{73}{44}=\frac{x}{4.4g}$ x=7.3g
盐酸溶液中溶质的质量分数为$\frac{7.3g}{55.5g}×$100%≈13.2%.
(2)$\frac{117}{44}=\frac{y}{4.4g}$ y=11.7g
$\frac{106}{44}=\frac{z}{4.4g}$ z=10.6g
反应后所得溶液中溶质的质量分数为$\frac{11.7g+16.9g-10.6g}{16.9g+55.5g-4.4g}$×100%≈26.5%.
答:(1)盐酸溶液中溶质的质量分数为13.2%;
(2)反应后所得溶液中溶质的质量分数为26.5%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
3.把一定质量的纯净物甲和40g的纯净物乙,恰好完全反应生成44g丙物质和9g丁物质(该反应的微观模型图见图).关于该反应的说法正确的是( )
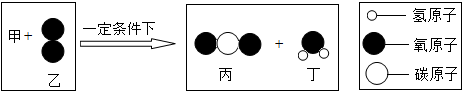

| A. | 甲为含氧化合物 | B. | 乙和丙的分子个数比为1:2 | ||
| C. | 甲分子中原子个数比为1:1 | D. | 丁中氢元素的质量为2g |
20.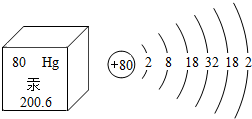 如图为汞元素的信息,下列说法正确的是( )
如图为汞元素的信息,下列说法正确的是( )
 如图为汞元素的信息,下列说法正确的是( )
如图为汞元素的信息,下列说法正确的是( )| A. | 汞的中子数为80 | |
| B. | 汞属于非金属元素 | |
| C. | 汞的相对原子质量为200.6g | |
| D. | 在化学反应中,汞原子容易失去电子 |
7.下表中除去物质中所含少量杂质的方法正确的是( )
| 选项 | 物质 | 所含杂质 | 除杂质的方法 |
| A | N2 | CO | 通过灼热的CuO |
| B | NaCl | Na2CO3 | 加入足量的稀盐酸充分反应后蒸发结晶 |
| C | KCl | MnO2 | 加水充分溶解,过滤、洗涤、干燥 |
| D | CaO | Ca(OH)2 | 加适量的水,干燥 |
| A. | A | B. | B | C. | C | D. | D |
4.下列实验现象的叙述中,错误的是( )
| A. | 细铁丝在氧气中剧烈燃烧,火星四射,放出热量,生成黑色固体 | |
| B. | 氨气使湿润的蓝色石蕊试纸变红 | |
| C. | 加热“铜绿”时,绿色固体变成黑色固体,管壁出现小水珠 | |
| D. | 向氯化钠溶液中滴加硝酸银溶液,生成白色沉淀 |
3.化学用语是世界通用的化学语言.有关物质的化学符号书写正确的是( )
| A. | 氯化亚铁:FeCl3 | B. | 碳酸钠:NaCO3 | C. | 水银:Hg | D. | 二氧化硫:SiO2 |
 如图甲、乙是实验室常用的两套气体制备、收集、检验的多种功能装置.
如图甲、乙是实验室常用的两套气体制备、收集、检验的多种功能装置.
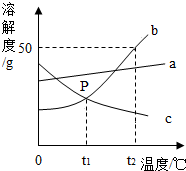 根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据图中a、b、c三种物质的溶解度曲线,回答下列问题: