题目内容
13.向足量的稀盐酸中加入10克铜锌合金.反应后得到0.2克氢气.求铜锌合金中锌的质量分数.分析 铜不能和稀盐酸反应,锌和稀盐酸反应生成氯化锌和氢气,根据氢气的质量可以计算锌的质量,进一步可以计算铜锌合金中锌的质量分数.
解答 解:设锌的质量为x,
Zn+2HCl═ZnCl2+H2↑,
65 2
x 0.2g
$\frac{65}{x}$=$\frac{2}{0.2g}$,
x=6.5g,
铜锌合金中锌的质量分数为:$\frac{6.5g}{10g}$×100%=65%,
答:铜锌合金中锌的质量分数为65%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
3.除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
| 物质 | 杂质 | 除杂所用试剂和方法 | |
| A | O2 | HCl气体 | 先通过NaOH溶液,再通过浓硫酸 |
| B | NaOH | Ca(OH)2溶液 | 先加入过量的Na2CO3溶液,再过滤 |
| C | NaCl | Na2CO3 | 加入澄清的石灰水,过滤 |
| D | CaO | CaCO3 | 加入适量的稀盐酸,蒸发 |
| A. | A | B. | B | C. | C | D. | D |
4.化学中常常出现“1+1≠2”的有趣现象,但也有例外,下列符合“1+1=2”的事实是( )
| A. | 20℃,1 L水与1 L酒精混合后的体积等于2 L | |
| B. | 20℃,1 g过氧化氢溶液和1 g二氧化锰混合充分反应后,剩余物质的总质量为2 g | |
| C. | 20℃,1 g镁在1 g氧气中燃烧会得到2 g氧化镁 | |
| D. | 20℃,1 g硫粉在1 g氧气中完全燃烧后生成2 g二氧化硫 |
8.组成硫酸亚铁的各元素,化合价最低和最高的分别是( )
| A. | 铁和氧 | B. | 氧和硫 | C. | 铁和硫 | D. | 氧和铁 |
2.类推是学习中所用的思维方法,下列类推结果错误的是( )
①酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应.
②氯化钠的水溶液显中性,所以盐溶液一定都显中性
③分子可以构成物质,物质一定是由分子构成的
④有机物都含碳元素,所以含碳元素的化合物都是有机物.
①酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应.
②氯化钠的水溶液显中性,所以盐溶液一定都显中性
③分子可以构成物质,物质一定是由分子构成的
④有机物都含碳元素,所以含碳元素的化合物都是有机物.
| A. | ① | B. | ①②③ | C. | ②③④ | D. | ①②③④ |
3.用氯化钠配制100克溶质质量分数为20%的氯化钠溶液,现有下列操作:①溶解,②称取氯化钠;③过滤;④量取水;⑤计算;⑥蒸发结晶.针对该实验说法正确的是( )
| A. | 正确的操作顺序是⑤②④①③⑥ | |
| B. | 直接在量筒中溶解配制溶液可减小误差 | |
| C. | 直接在天平上称取20g氯化钠 | |
| D. | 配制时用量筒量取80毫升蒸馏水 |
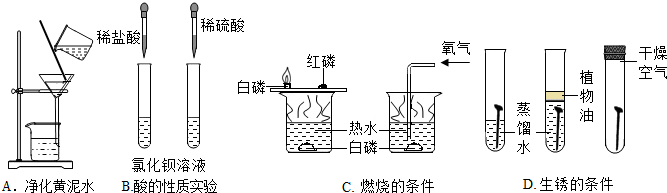 (1)用A图所示装置净化黄泥水时,玻璃棒的作用是引流.
(1)用A图所示装置净化黄泥水时,玻璃棒的作用是引流.